Onderwerpen
Hoofdstuk 3 - Voortzetting en afronding van het OPAT-traject
- 3.1 - Monitoring op effectiviteit en bijwerkingen
- 3.1.1 - De infectieziekte: respons en behandelduur
- 3.1.2 - Intraveneuze toegang en toediening antimicrobiële middelen
- 3.1.3 - Bijwerkingen
- 3.1.4 - Therapeutic drug monitoring
- 3.1.5 - Medicatiebewaking
- 3.2 - Zelftoediening (S-OPAT)
- 3.2.1 - Organisatie van zelftoediening
- 3.2.2 - Training van patiënten
- 3.2.3 - Implementatie
- 3.2.4 - Monitoring en evaluatie
- 3.3 - Hygiëne en infectiepreventie na ontslag
- 3.3.1 - Wijkverpleging
- 3.3.2 - Patiënt
- 3.3.3 - Dragerschap van Bijzonder Resistente Micro-Organismen (BRMO) en MRSA
- 3.4 - Afronding van het OPAT-traject
- Literatuur
- ↑ Naar boven
Naar ander hoofdstuk:
- Hoofdstuk 1 - Organisatie van een OPAT-programma
- Hoofdstuk 2 - Initiatie van OPAT
- Hoofdstuk 4 - Communicatie tussen zorgverleners gedurende het OPAT-traject
- Hoofdstuk 5 - Aandachtspunten bij kinderen
- Hoofdstuk 6 - Bewaken van de kwaliteit van zorg voor OPAT-patiënten
- Hoofdstuk 7 - Bijlagen
3.1 - Monitoring op effectiviteit en bijwerkingen
|
|
De aard van OPAT in de thuissituatie vraagt om enkele specifieke aandachtspunten
die gemonitord en gedocumenteerd dienen te worden:
- De infectieziekte waarvoor OPAT is gestart
- De respons van de infectieziekte op de ingestelde behandeling
- Het bepalen van een stopdatum of herbeoordelingsmoment
- Intraveneuze toegang en toediening antimicrobiële therapie
- Functioneren van de intraveneuze toegang
- Hoe de intraveneuze toedieningen verlopen
- Bijwerkingen van de antimicrobiële therapie
- Secundaire infecties, zoals C. difficile colitis en lijngerelateerde infecties
- Bijwerkingen, zoals gastro-intestinale klachten, allergische reacties of gehoorverlies
- Afwijkende laboratoriumwaarden
- Therapeutic drug monitoring (TDM) indien van toepassing
- Medicatiebewaking
- Bewaking op geneesmiddelinteracties
- Dosisaanpassing bij verandering van de nierfunctie
Monitoren van dergelijke aandachtspunten kan helpen bij het voorkomen van heropnames tijdens OPAT. Daarnaast draagt een vroege poliklinische controle (binnen twee weken na ontslag) hier ook aan bij. In de literatuur worden bij OPAT-patiënten desondanks heropnamepercentages tot ~20% worden gerapporteerd. Heropnames zijn vaak ziekte- of OPAT-gerelateerd en vinden frequenter plaats in de eerste weken na ontslag. Door tijdige interventies kunnen deze heropnames deels worden voorkomen. Patiëntfactoren die geassocieerd zijn met heropname staan weergegeven in tabel 3.1. Deze patiëntgebonden factoren kunnen derhalve sturend zijn bij het bepalen van de intensiteit van de controles.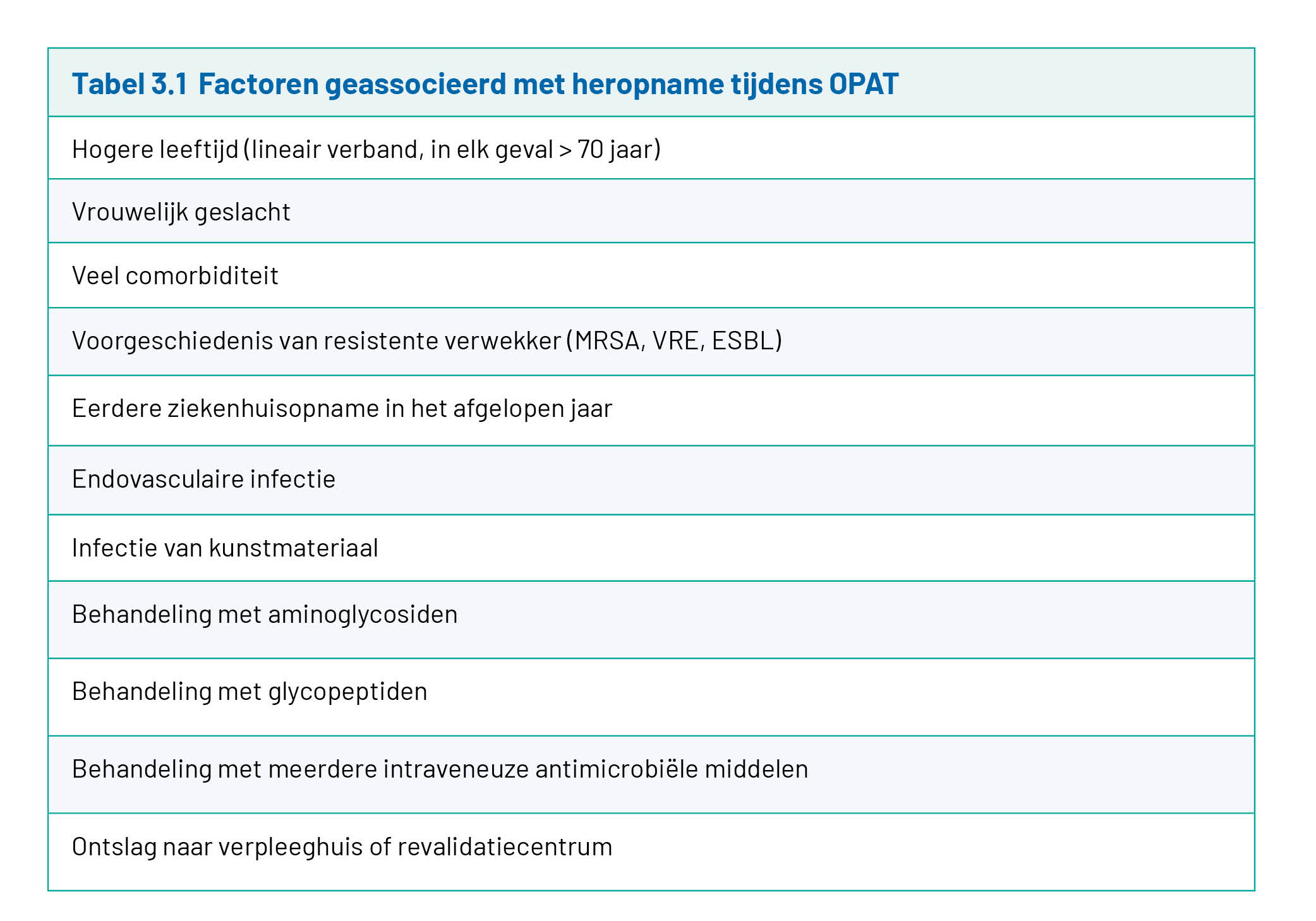
3.1.1 - De infectieziekte: respons en behandelduur
De monitoringsfrequentie van de respons van de infectieziekte op de ingestelde behandeling zal erg afhangen van het type infectie en de klinische toestand van de patiënt en zijn niet te vangen in een algemene richtlijn. Actieve begeleiding van patiënten die OPAT ontvangen waarbij ten tijde van de start van de behandeling nog geen stopdatum bekend is, leidt tot tijd- en kostenbesparing.
3.1.2 - Intraveneuze toegang en toediening antimicrobiële middelen
Zowel de wijkverpleging als het OPAT-team hebben een rol bij het monitoren van eventuele problemen bij de toediening en het functioneren van de intraveneuze toegang. De wijkverpleging kan bij elk bezoek de lijn en het correct inlopen van het antimicrobiële middel controleren. Vanuit het ziekenhuis kunnen deze aspecten goed telefonisch besproken worden. Deze actieve monitoring heeft toegevoegde waarde naast duidelijke instructies aan de patiënt om bij problemen contact op te nemen. Aan het einde van de therapie dient de intraveneuze toegang – indien niet meer nodig voor andere doeleinden – verwijderd te worden. De wijkverpleging kan dit in het geval van een perifeer infuus, PICC of midline doen, mits hiervoor opdracht gegeven is (zie hoofdstuk 2.6 Het aanvraagproces).
3.1.3 - Bijwerkingen
Bijwerkingen en secundaire infecties
De patiënt dient zoals beschreven in hoofdstuk 2.5 geïnformeerd te zijn over veelvoorkomende bijwerkingen en wanneer hij/zij hierbij actie dient te ondernemen. Bij de eerste gift van een antimicrobieel middel dient gemonitord te worden of er geen anafylactische reactie plaatsvindt, ook als OPAT poliklinisch of op de SEH geïnitieerd wordt, zie hoofdstuk 2.2. Tijdens het verdere verloop van OPAT heeft, naast de patiënt zelf, de wijkverpleging ook een belangrijke signalerende functie. Het dient duidelijk te zijn voor de patiënt en wijkverpleging wie de hoofdverantwoordelijke van het ingestelde OPAT-traject in het ziekenhuis is, zodat de melding van eventuele bijwerkingen geen vertraging oploopt. Daarnaast dient actief navraag naar bijwerkingen gedaan te worden bij de (telefonische) controles die vanuit het ziekenhuis gepland staan. De meeste bijwerkingen zullen zich in het begin van de behandeling openbaren, dus ook hiervoor geldt dat een evaluatie hiervan kort na start van de therapie zinvol is. OPAT is op zichzelf een risicofactor voor bepaalde secundaire infecties zoals C. difficile colitis en lijngerelateerde infecties. Patiënten dienen geïnformeerd te zijn over de klachten die op secundaire infecties kunnen wijzen. Tevens dienen deze klachten actief uitgevraagd te worden tijdens contact met de patiënt.
Afwijkende laboratoriumwaarden
Bijwerkingen door antimicrobiële middelen komen bij OPAT frequent voor. Het structureel monitoren van eventuele bijwerkingen door middel van laboratoriumbepalingen is geassocieerd met minder heropnames. Data ontbreken echter die beschrijven hoe frequent deze bepalingen gedaan dienen te worden. Bij gebrek aan bewijs adviseert de IDSA-richtlijn bij de meeste middelen om ten minste wekelijks uitgebreid bloedonderzoek te laten verrichten. Gebaseerd op deze richtlijn en artikelen die de frequentie en ernst van bijwerkingen beschrijven voor de meest gebruikte medicatie in Nederland, is een tabel gemaakt die een leidraad kan vormen voor de frequentie van laboratoriumcontroles (tabel 3.2). Op basis van individuele patiëntkenmerken die het risico op afwijkende laboratoriumwaarden beïnvloeden (bijvoorbeeld comorbiditeit) is afwijken van deze leidraad zeer wel denkbaar. Daarnaast dient opgemerkt te worden dat de meeste bijwerkingen vermoedelijk in de eerste twee weken optreden en verruiming van de intervallen bij lange behandeling gerechtvaardigd lijkt.
Eosinofilie is een frequent optredende bijwerking van intraveneuze antimicrobiële therapie. Een studie liet zien dat 25% van de patiënten eosinofilie ontwikkelden, veelal mild. Penicillines en vancomycine veroorzaken het meest frequent eosinofilie. Het belang van het vaststellen van eosinofilie is dat het geassocieerd is met een verhoogd risico op (toekomstige) overgevoeligheidsreacties. Ongeveer 30% van de patiënten met eosinofilie ontwikkelt een overgevoeligheidsreactie en eosinofilie is een onafhankelijke voorspeller van nierfunctiestoornissen en huiduitslag. Voor de praktijk betekent dit dat eosinofilie op zich geen reden is om de therapie te staken, maar dat alertheid geboden is op eventuele overgevoeligheidsreacties. Een bijzondere vermelding in dit kader betreft de relatief zeldzame maar ernstige type-IV allergie DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms), waarbij patiënten naast eosinofilie en huiduitslag, ook koorts en vaak lymfadenopathie, orgaanbetrokkenheid zoals leverfunctiestoornissen of longafwijkingen hebben. Hierbij dient het antibioticum direct gestaakt te worden en is vaak immuunsuppressie nodig.
Bij het vormgeven van de laboratoriumcontroles dient er niet alleen zorg voor worden gedragen dat bloed geprikt wordt. Even belangrijk is het om ervoor te zorgen dat de uitslagen bij de verantwoordelijke zorgverlener terechtkomen. Helaas gaat dit in de praktijk geregeld verkeerd. Het beleggen van deze verantwoordelijkheid bij het OPAT-team zal dit deels verbeteren, maar het blijft een logistieke uitdaging om controles op een betrouwbare en efficiënte wijze vorm te geven, zeker bij patiënten van buiten de regio van het ziekenhuis. Thuisafnameservices of afname bij lokale prikposten middels opgestuurde afnamesetjes waarbij de buisjes naar het ziekenhuislaboratorium worden opgestuurd, kunnen een oplossing bieden, mits de transporttijd acceptabel is. Daarnaast zijn er ziekenhuizen die via het EPD rechtstreeks toegang hebben tot de laboratoriumuitslagen van bepaalde externe laboratoria, zoals huisartsenlaboratoria en andere ziekenhuizen.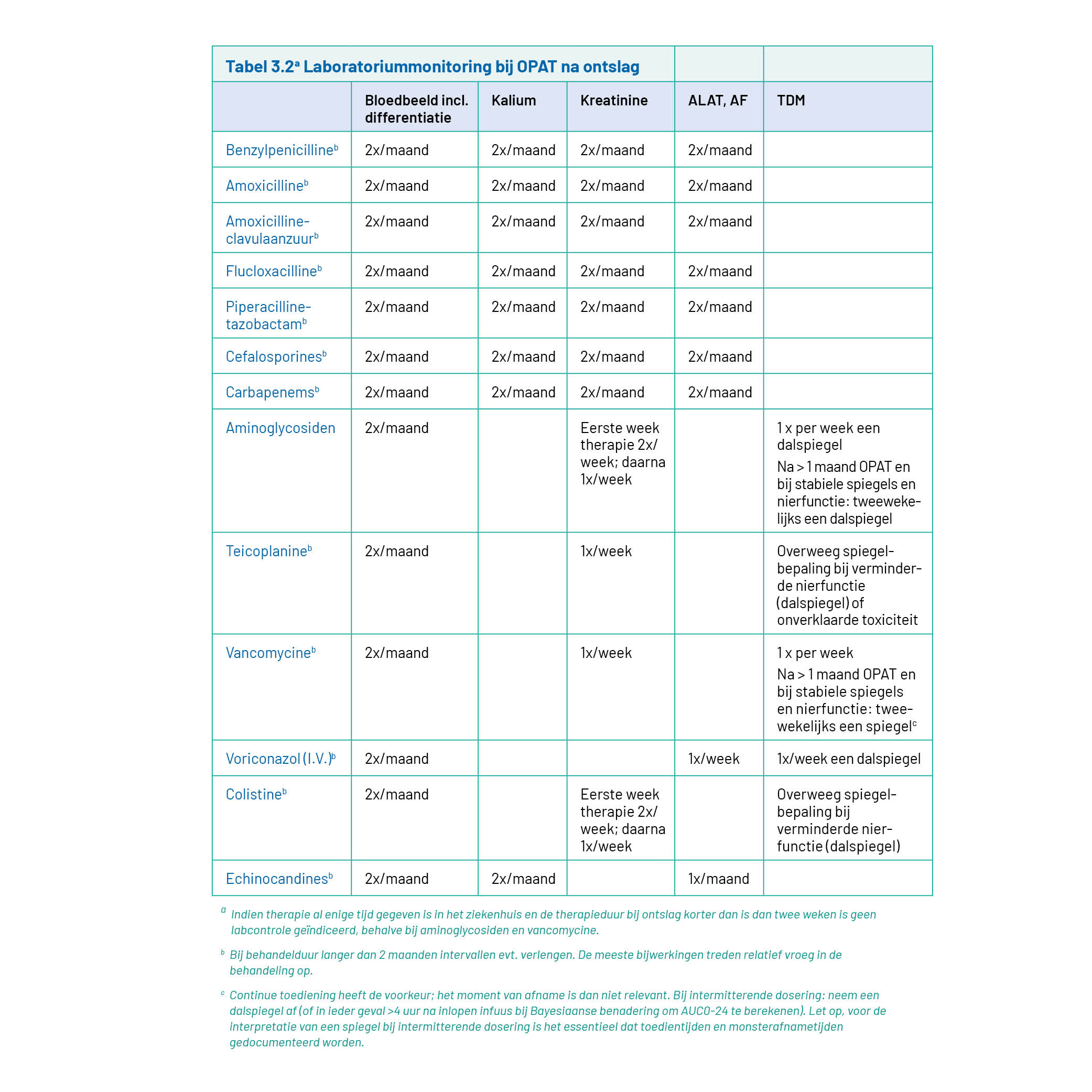
3.1.4 - Therapeutic drug monitoring
De optimale dosering van bepaalde antimicrobiële middelen kan voor een individuele patiënt worden vastgesteld op geleide van de geneesmiddelconcentratie in plasma. Dit wordt therapeutic drug monitoring (TDM) genoemd. Wie de verantwoordelijkheid draagt voor het uitvoeren van TDM dient te worden afgesproken. Dit kan zowel de hoofdbehandelaar als het OPAT-team zijn. De (ziekenhuis-)apotheker adviseert over de uit te voeren laboratoriumbepalingen, het gewenste afnamemoment en geeft doseringsadviezen op basis van de uitslagen.
In de Nederlandse praktijk wordt TDM veelal toegepast bij het gebruik van aminoglycosiden, vancomycine en IV voriconazol. TDM kan daarnaast overwogen worden bij andere antimicrobiële middelen zoals onder andere teicoplanine en colistine. Vancomycine en aminoglycosiden worden in principe gestart tijdens een klinische opname. Het is aan te bevelen om, voorafgaand aan ontslag met OPAT, ervoor te zorgen dat er sprake is van een stabiele geneesmiddelconcentratie in het therapeutisch gebied die naar verwachting aanhoudt tijdens OPAT (op basis van modellering). Anticiperend hierop is het raadzaam om al ruim voor ontslag over te gaan op continue toediening van vancomycine, zoals dat in de thuissituatie ook gegeven wordt. Er kan dan bijvoorbeeld gestreefd worden naar twee opeenvolgende therapeutische concentraties bij eenzelfde dosering.
Ook na ontslag met OPAT is het belangrijk om geneesmiddelspiegels te blijven monitoren. Prospectieve studies naar de optimale frequentie van TDM gedurende OPAT ontbreken. Diverse bronnen houden een frequentie aan van (minimaal) 1 keer per week. Daarnaast wordt ook beschreven dat bij langdurige OPAT-trajecten, na 1 maand de frequentie gereduceerd kan worden naar 2 keer per maand in geval van stabiele spiegels. In tabel 3.2 is voor diverse antimicrobiële middelen weergegeven wanneer TDM overwogen kan worden. Het is belangrijk om te benoemen dat er, zeker wanneer het gaat over andere middelen dan vancomycine en aminoglycosiden, verschillen in beleid kunnen bestaan tussen ziekenhuizen. In tabel 3.2 is voor de overige middelen dan ook aangegeven in welke situaties TDM overwogen dient te worden. Het is belangrijk dat hier binnen het ziekenhuis afspraken over gemaakt worden, bijvoorbeeld in een richtlijn of een SOP.
3.1.5 - Medicatiebewaking
Tijdens OPAT is het, net als bij andere medicamenteuze behandelingen, belangrijk om gedurende de gehele behandeling te monitoren op geneesmiddelinteracties bij wijzigingen in de medicatie, zowel door de voorschrijver als door de apotheker. Daarnaast dient beoordeeld te worden of er dosiswijzigingen noodzakelijk zijn bij achteruitgang of verbetering van de nierfunctie (voor renaal geklaarde middelen).
3.2 - Zelftoediening (S-OPAT)
|
|
In Nederland wordt de toediening van intraveneuze antimicrobiële middelen bij patiënten thuis voornamelijk uitgevoerd door gespecialiseerde verpleegkundigen van de wijkverpleging. Dit houdt in dat, gedurende de gehele duur van OPAT, verpleegkundigen van de wijkverpleging minimaal één keer per dag –en afhankelijk van het middel, frequenter– bij patiënten langsgaan om de antimicrobiële middelen toe te dienen en de intraveneuze toegang te verzorgen. Dit betekent dat er een groot beroep gedaan wordt op thuiszorgorganisaties. Antimicrobiële middelen die een korte houdbaarheid hebben en waarbij de houdbaarheid niet verlengd kan worden bijvoorbeeld door de oplossing te bufferen, zoals amoxicilline en imipenem/cilastatine, dienen meerdere keren per dag toegediend te worden; soms vaker dan de zorgcapaciteit toestaat. Daarnaast beperkt de afhankelijkheid van de wijkverpleging de vrijheid van de patiënt, een waarde die volgens de patiënt centraal zou moeten staan bij OPAT. Zelftoediening door patiënten of mantelzorgers kan dan ook een interessant alternatief zijn. Verschillende studies hebben al aangetoond dat zelftoediening veilig is, niet leidt tot meer heropnames of complicaties en dat het de patiënttevredenheid en autonomie bevordert. Zelftoediening wordt eenvoudiger gemaakt door het gebruik van patiëntvriendelijke toedieningssystemen, zoals elastomeerpompen, medicatiecassettes en draagbare infuuspompen.
3.2.1 - Organisatie van zelftoediening
Zelftoediening vindt op dit moment (2022) in beperkte mate plaats in Nederland. Het wordt namelijk maar in 30% van de Nederlandse ziekenhuizen aangeboden. De perceptie is dat zelftoediening vaak gedaan wordt door jonge mensen die langdurig en/of bij herhaling antimicrobiële middelen nodig hebben. Echter is de groep aan wie zelftoediening wordt aangeboden tegenwoordig veel breder, met ook oudere patiënten die er cognitief en fysiek nog toe in staat zijn, en patiënten die maar kort OPAT krijgen. Voordat zelftoediening structureel aangeboden kan worden, dient een OPAT-team een aantal randvoorwaarden op te stellen.
Richtlijnen beschrijven geen criteria waaraan een patiënt moet voldoen om de toedieningen in de thuissituatie zelf te doen. Wel zijn de literatuur en experts het erover eens dat de aspecten die genoemd staan in tabel 3.3 handvatten zijn om een individuele afweging te maken. Patiënten kunnen al vóór ontslag voor zelftoediening geselecteerd worden.
3.2.2 - Training van patiënten
De patiënt en/of mantelzorger dient getraind te worden voordat met zelftoediening wordt gestart. Zelftoediening kan volledig in het ziekenhuis, volledig bij de patiënt thuis of in beide omgevingen aangeleerd worden. Het is niet wenselijk dat patiënten langer opgenomen moeten blijven in het ziekenhuis om de training af te ronden. Indien de training nog niet is afgerond in het ziekenhuis kan de wijkverpleging de eerste dagen OPAT toedienen en, indien mogelijk, de training afronden. Ook is het mogelijk dat in de thuissituatie pas gestart wordt met het aanleren van zelftoediening. In de praktijk is namelijk te merken dat patiënten soms enigszins overweldigd zijn door alle informatie in het ziekenhuis, en OPAT liever eerst even aankijken thuis, terwijl het nog door de wijkverpleging wordt toegediend.
Aangezien de locatie van het aanleren kan verschillen, is het daarvan afhankelijk wie de handelingen leert aan de patiënt en/of mantelzorger. Dit kunnen dus verpleegkundigen van de afdeling zijn, OPAT-verpleegkundigen in het ziekenhuis, de wijkverpleging, verpleegkundigen van een organisatie gericht op het aanleren van handelingen aan een patiënt, of een combinatie hiervan. Een organisatie gericht op het aanleren van handelingen aan patiënten kan een grote toegevoegde (didactische) waarde hebben bij het ontwikkelen en geven van training voor zelftoediening van OPAT. Een voorbeeld hiervan is de Academie voor Patiënt en Mantelzorger in het Maastricht UMC+. Voor het aanleren van de zelftoediening gebruiken zij het stappenplan dat ook wordt gebruikt voor het aanleren van reanimeren, zie figuur 3.1.
Een ander voorbeeld is APPO, de apotheek die voor enkele ziekenhuizen in (o.a. Amsterdam UMC) de antibiotica, pomp en overige materialen aan OPAT-patiënten levert. Zij hebben verpleegkundigen in dienst die patiënten in het ziekenhuis of in de thuissituatie dergelijke verpleegtechnische handelingen aanleert, middels hetzelfde stappenplan.
Bij het aanleren van zelftoediening kijkt de patiënt of mantelzorger dus eerst enkele keren mee met de verpleegkundige, waarna onder supervisie de zelftoediening zal plaatsvinden. Pas nadat zowel de patiënt als de verpleegkundige overtuigd zijn van de vaardigheden van de zelftoediener kan de training afgesloten worden. Naast het aanleren van de handelingen die verricht moeten worden, moet er ook scholing plaatsvinden over de mogelijke complicaties en hoe te handelen bij specifieke situaties.
Twee voorbeelden van geschreven handleidingen voor zelftoediening van OPAT middels elastomeerpompen staan in bijlage 4. Eén voorbeeld van een handleiding voor S-OPAT met medicatiecassettes staat in bijlage 5. Patiënten geven vaak de voorkeur aan video-instructies boven geschreven handleidingen. Mediq heeft Nederlandstalige filmpjes en handleidingen voor verschillende pompen ontwikkeld voor het zelfstandig aansluiten van infuuszakken, medicatiecassetten en elastomeerpompen, net als het eerder genoemde APPO, zie https://mediq.nl/patient/infuus. Ook zijn er Engelstalige voorbeelden van filmpjes beschikbaar met instructies voor zelftoediening door de patiënt, te vinden via de link https://e-opat.com/infectious-disease-videos/. Eventueel kunnen ook de trainingen van de patiënt opgenomen worden, zodat hij/zij deze later in eigen tijd terug kan kijken in geval van twijfels of onzekerheden.
3.2.3 - Implementatie
Indien zowel de patiënt als de gespecialiseerd verpleegkundige overtuigd zijn van de bekwaamheid van de patiënt of mantelzorger, kan gestart worden met zelftoediening. Aanbevolen wordt om schriftelijk vast te leggen dat de patiënt training heeft doorlopen en akkoord is met de zelftoediening. De wijkverpleging vraagt hiervoor ook toestemming aan de hoofdbehandelaar, indien niet vooraf gegeven. Idealiter heeft dit al plaatsgevonden bij initiatie van OPAT in het ziekenhuis.
Ook dient, indien noodzakelijk, het wekelijkse bezoek van de wijkverpleging voor de verzorging van de intraveneuze toegang geregeld te zijn, en de achterwachtfunctie die zij gedurende de week hebben.
3.2.4 - Monitoring en evaluatie
Afhankelijk van de geldende protocollen binnen de thuiszorgorganisaties volgt er 1-2x per week een bezoek van een verpleegkundige voor het evalueren en verzorgen van de intraveneuze toegangsweg en het zo nodig vervangen van de verlenglijn. Hierbij kan, indien nodig, ook de handeling van de antibiotica zelf toedienen geëvalueerd worden, en eventuele vragen beantwoord.
De patiënt zal zelf dagelijks de insteek inspecteren en weet wanneer hij contact moet opnemen met de wijkverpleging. In tabel 3.4 zijn, gebaseerd op een Vilans protocol, voorbeelden beschreven van potentiële complicaties waarbij de patiënt contact dient op te nemen met de wijkverpleging of behandelend arts. Vilans is een landelijke kennisorganisatie voor zorg en ondersteuning.
Voor dergelijke complicaties en andere problemen is het van belang dat er een achterwachtfunctie is toegewezen aan een thuiszorgorganisatie. 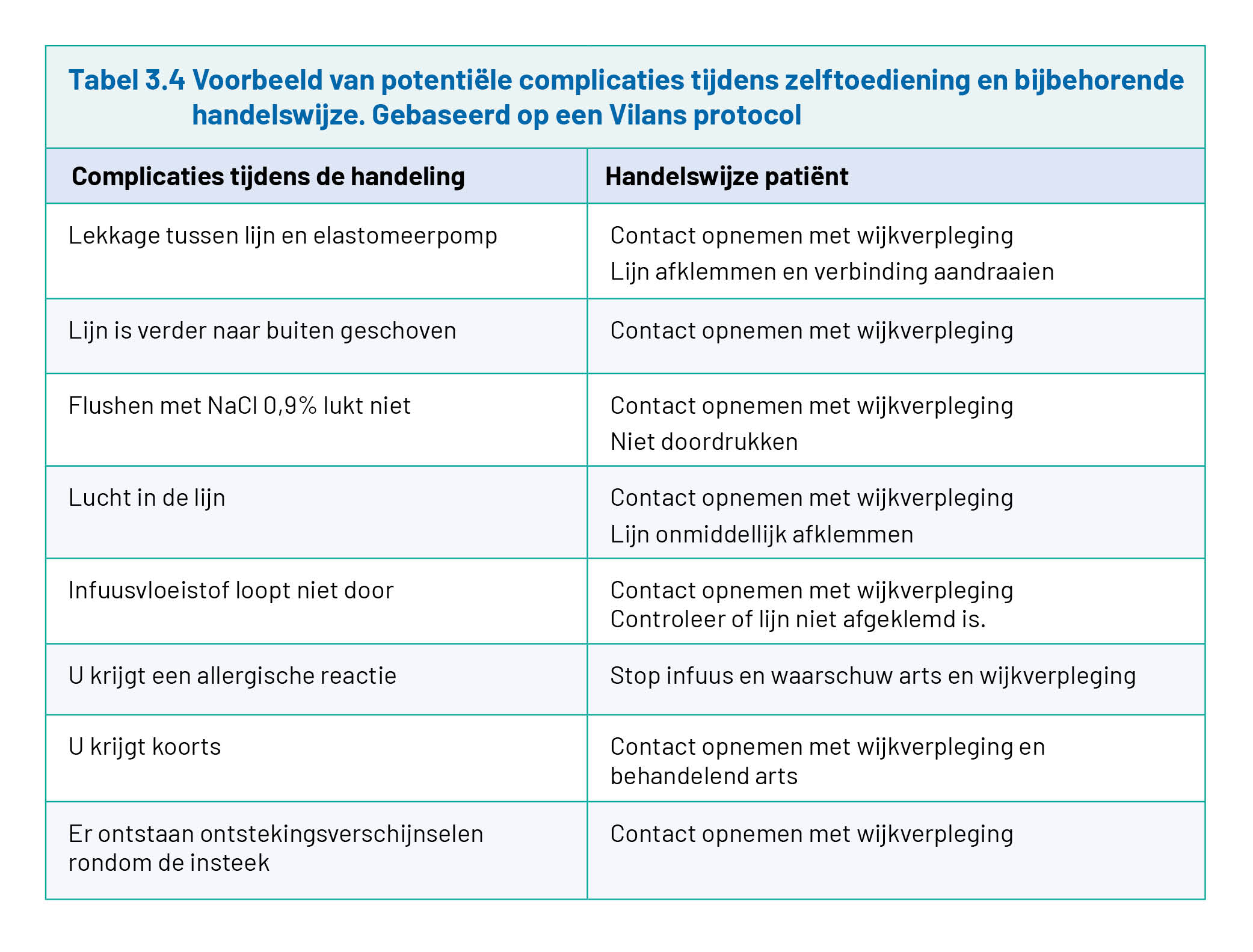
3.3 - Hygiëne en infectiepreventie na ontslag
|
|
OPAT-patiënten zijn extra vatbaar voor infecties vanwege de aanwezigheid van een intraveneuze toegang waardoor dagelijks toedieningen plaatsvinden. Een hygiënische manier van werken is derhalve cruciaal. Bovendien is een uniforme en hygiënische werkwijze belangrijk voor het gevoel van veiligheid van patiënten. Daarnaast is er bij OPAT-patiënten relatief vaak sprake van dragerschap of een infectie met een resistent micro-organisme. De meeste patiënten zijn namelijk recent uit het ziekenhuis ontslagen of krijgen intraveneuze antimicrobiële middelen omdat orale opties niet beschikbaar zijn vanwege resistentie.

3.3.1 - Wijkverpleging
Wat betreft persoonlijk hygiëne gelden de vigerende infectiepreventieprotocollen zoals die door verschillende organisaties en instellingen opgesteld zijn. Uitgebreide instructies zijn vindbaar in de Vilans- en instellingsprotocollen. Bij handelingen die bij infuustherapie uitgevoerd worden geldt dat de handen altijd gedesinfecteerd dienen te worden met handenalcohol. Voor handelingen bij infuustherapie (bereidingen van antimicrobiële middelen, toedieningen, lijnverzorging, etc.) wordt in het ziekenhuis vaak een steriel werkveld gecreëerd. In de thuissituatie werkt men met schone velden. Voor het inrichten van zowel een steriel werkveld als een schoon werkveld zijn protocollen. Of de handeling met steriele handschoenen moet worden verricht wordt bepaald door het ziekenhuis, ook als de patiënt in de thuissituatie wordt behandeld. Zo nee, dan wordt de no-touch techniek gebruikt. Het wordt ook in het ziekenhuis steeds gebruikelijker om de no-touch techniek toe te passen in plaats van steriel werken. Voor de verzorging van de lijn en toediening van medicatie kunnen bijvoorbeeld protocollen van Vilans of van de eigen instelling gebruikt worden.
3.3.2 - Patiënt
Ook van de patiënt wordt persoonlijke hygiëne verwacht en daarover dient de patiënt te worden geïnformeerd. Voor de wijkverpleging betekent dit dat de werkomgeving waar de handelingen plaatsvinden schoon en opgeruimd dient te zijn. De infuusmaterialen moeten in een af te sluiten doos bewaard worden. Huisdieren horen tijdens de handelingen uit de buurt te worden gehouden.
3.3.3 - Dragerschap van Bijzonder Resistente Micro-Organismen (BRMO) en MRSA
BRMO-dragerschap dient bij overdracht naar de wijkverpleging direct te worden vermeld, zodat maatregelen als het dragen van beschermende kleding en materialen (bijv. bij MRSA), tijdig genomen kunnen worden. Thuis moeten deze materialen niet in dezelfde ruimte als waar de patiënt zich bevindt, bewaard worden. Zie: https://www.rivm.nl/brmo en https://www.rivm.nl/vragen-en-antwoorden-brmo. Informatiefilms en – folders voor patiënten zijn te vinden op: https://www.zorgnetwerk-gain.nl/public/nascholing/voorlichtingsmateriaal/. Ook zijn er landelijke transmurale werkafspraken gemaakt over zorg voor patiënten met een BRMO, zie https://www.abrzorgnetwerkutrecht.nl/wp-content/uploads/2020/11/Landelijke-Transmurale-Werkafspraken.pdf. Deze werkafspraken hebben als doel om de transmurale informatieoverdracht bij overplaatsing tussen zorgorganisaties van dragers met een BRMO te verbeteren. Het document kan als een eenduidige landelijke werkwijze voor de transmurale overdracht over BRMO te dienen, inclusief praktische handreikingen in de vorm van drie veel voorkomende situaties. Uiteindelijk draagt dit bij aan het voorkomen van verspreiding van BRMO’s en van toename van antibioticaresistentie.
3.4 - Afronding van het OPAT-traject
Aan het einde van het OPAT-traject is het belangrijk om een aantal zaken af te ronden. De intraveneuze toegang dient te worden verwijderd tenzij er een andere reden is om deze te behouden. Daarnaast dienen zorgverleners elkaar, zoals in hoofdstuk 4 beschreven is, te informeren over de afronding van het OPAT-traject. Tevens is het goed om de tevredenheid en ervaringen van patiënten te evalueren, waar ook verder op in wordt gegaan in hoofdstuk 6.3.
Literatuur
- Blumenthal KG, Youngster I, Rabideau DJ et al. Peripheral blood eosinophilia and hypersensitivity reactions among patients receiving outpatient parenteral antibiotics. J Allergy Clin Immunol. 2015 Nov;136(5):1288-94.e1. doi: 10.1016/j.jaci.2015.04.005.
- Browning S, Loewenthal MR, Freelander I et al. Safety of prolonged outpatient courses of intravenous antibiotics: a prospective cohort study. Clin Microbiol Infect. 2022 Jun;28(6):832-837. doi: 10.1016/j.cmi.2021.12.020.
- Chapman ALN, Patel S, Horner C, Gilchrist M et al. Outpatient parenteral antimicrobial therapy: updated recommendations from the UK. J Antimicrob Chemother. 2019 Nov 1;74(11):3125-3127. doi: 10.1093/jac/dkz343
- De Velde, F, Mouton JW, de Winter BCM et al. “Clinical applications of population pharmacokinetic models of antibiotics: Challenges and perspectives.” Pharmacol Res 134: 280-288. doi: 10.1016/j.phrs.2018.07.005.
- Douiyeb S, de la Court JR, Tuinte B et al. Risk factors for readmission among patients receiving outpatient parenteral antimicrobial therapy: a retrospective cohort study. Int J Clin Pharm. 2022 Apr;44(2):557-563. doi: 10.1007/s11096-022-01379-7.
- Frisby J, Ali N, Niemotka S, Abate G. Usefulness of Routine Laboratory Tests for Follow up of Patients Receiving Outpatient Parenteral Antimicrobial Therapy Run by Infectious Diseases Fellows. Antibiotics (Basel). 2023 Feb 4;12(2):330. doi: 10.3390/antibiotics12020330.
- Handbook of; Outpatient Parenteral Antimicrobial Therapy For Infectious Diseases; 3ed. 2016 CRG Publishing, Division of The Curry Rockefeller Group, LLC, and the Infectious Diseases Society of America. https://www.idsociety.org/opat-ehandbook/
- Huck D, Ginsberg JP, Gordon SM et al. Association of laboratory test result availability and rehospitalizations in an outpatient parenteral antimicrobial therapy programme. J Antimicrob Chemother. 2014 Jan;69(1):228-33. doi: 10.1093/jac/dkt303.
- Keller SC, Williams D, Gavgani M et al. Rates of and Risk Factors for Adverse Drug Events in Outpatient Parenteral Antimicrobial Therapy. Clin Infect Dis. 2018 Jan 6;66(1):11-19. doi: 10.1093/cid/cix733.
- Landelijk Centrum Hygiëne en Veiligheid (2016). Hygiënerichtlijn voor verpleeghuizen, woonzorgcentra en kleinschalig wonen. Amsterdam: Landelijk Centrum Hygiëne en Veiligheid.
- Mitchell ED, Czoski Murray C, Meads D et al. Clinical and cost-effectiveness, safety and acceptability of community intravenous antibiotic service models: CIVAS systematic review. BMJ Open. 2017 Apr 20;7(4):e013560. doi: 10.1136/bmjopen-2016-013560.
- Norris AH, Shrestha NK, Allison GM et al. Infectious Diseases Society of America Clinical Practice Guideline for the Management of Outpatient Parenteral Antimicrobial Therapy. Clin Infect Dis. 2019 Jan 1;68(1):e1-e35. doi: 10.1093/cid/ciy745
- Palms DL, Jacob JT et al. Close Patient Follow-up Among Patients Receiving Outpatient Parenteral Antimicrobial Therapy. Clin Infect Dis. 2020 Jan 1;70(1):67-74. doi: 10.1093/cid/ciz150
- Regionale Zorgnetwerken Antibioticaresistentie. Landelijke transmurale werkafspraken Bijzonder Resistente Micro Organismen : Zorg voor een complete overdracht. Landelijke Transmurale Werkafspraken def versie okt 2020 (abrzorgnetwerkutrecht.nl)
- Stoorvogel HH, Hulscher MEJL, Wertheim HFL et al. Current practices and opportunities for outpatient parenteral antimicrobial therapy in hospitals: A national cross-sectional survey. Antibiotics. 2022 Oct;11(10):1343. doi: 10.3390/antibiotics11101343.
- Tonna A, Anthony G, Tonna I et al. Home self-administration of intravenous antibiotics as part of an outpatient parenteral antibiotic therapy service: a qualitative study of the perspectives of patients who do not self-administer. BMJ Open. 2019 Jan 25;9(1):e027475. doi: 10.1136/bmjopen-2018-027475.
- Werkgroep Infectie Preventie (2004). Verpleeghuis- woon- en thuiszorg : Handhygiëne. Leiden: Werkgroep Infectie Preventie.
- Werkgroep Infectie Preventie (2014). Persoonlijke hygiene [VWK]. Leiden: Werkgroep Infectie Preventie.
- Werkgroep Infectiepreventie. Handhygiëne. Ziekenhuizen. Oktober 2007- revisie oktober 2012.
Lees verder
- Hoofdstuk 1 - Organisatie van een OPAT-programma
- Hoofdstuk 2 - Initiatie van OPAT
- Hoofdstuk 4 - Communicatie tussen zorgverleners gedurende het OPAT-traject
- Hoofdstuk 5 - Aandachtspunten bij kinderen
- Hoofdstuk 6 - Bewaken van de kwaliteit van zorg voor OPAT-patiënten
- Hoofdstuk 7 - Bijlagen
- Download de OPAT praktijkgids
