Onderwerpen
Hoofdstuk 2 - Initiatie van OPAT
- 2.1 - Identificatie van klinische patiënten die in aanmerking komen voor OPAT
- 2.1.1 - Reactieve identificatie van patiënten
- 2.1.2 - Proactieve identificatie van patiënten
- 2.2 - Initiatie van OPAT op de spoedeisende hulp, dagbehandeling of polikliniek
- 2.2.1 - Initiatie op de spoedeisende hulp
- 2.3 - Beoordeling of OPAT een geschikte behandelwijze is
- 2.3.1 - Beoordeling door OPAT-team
- 2.3.2 - Beoordelingscriteria
- 2.4 - De selectie van het antimicrobiële middel
- 2.4.1 - De noodzakelijke toedieningsfrequentie
- 2.4.2 - Verschillende toedieningsvormen
- 2.5 - Het informeren van patiënten en mantelzorgers
- 2.6 - Het aanvraagproces
- 2.6.1 - Aanvraag plaatsing intraveneuze toegang
- 2.6.2 - Voorschrift voor medicatie
- 2.6.3 - Aanvraag voor nazorg door specialistisch team van de wijkverpleging
- 2.7 - Intraveneuze toegang
- 2.8 - Het opstellen van een behandelplan
- Literatuur
- ↑ Naar boven
Naar ander hoofdstuk:
- Hoofdstuk 1 - Organisatie van een OPAT-programma
- Hoofdstuk 3 - Voortzetting en afronding van het OPAT-traject
- Hoofdstuk 4 - Communicatie tussen zorgverleners gedurende het OPAT-traject
- Hoofdstuk 5 - Aandachtspunten bij kinderen
- Hoofdstuk 6 - Bewaken van de kwaliteit van zorg voor OPAT-patiënten
- Hoofdstuk 7 - Bijlagen
2.1 - Identificatie van klinische patiënten die in aanmerking komen voor OPAT
|
|
Er zijn verschillende manieren waarop patiënten die mogelijk in aanmerking komen voor OPAT onder de aandacht kunnen komen van het OPAT-team.
2.1.1 - Reactieve identificatie van patiënten
Van een reactieve identificatie van patiënten is sprake indien er een vraag van de hoofdbehandelaar is om OPAT te starten. Het OPAT-team dient dan na te gaan of OPAT inderdaad de beste keuze voor de patiënt is, en of er geen mogelijkheid is de antibiotica te staken dan wel oraal te behandelen. De criteria om te beoordelen of een patiënt in aanmerking komt voor OPAT zijn verderop in deze praktijkgids beschreven (hoofdstuk 2.3.2 Beoordelingscriteria).
2.1.2 - Proactieve identificatie van patiënten
Naast deze reactieve identificatie van patiënten kan het OPAT-team zelf proactief patiënten identificeren. Patiënten met gecompliceerde infecties, zoals gewrichtsprothese-infecties, vaatinfecties of endocarditis, worden veelal besproken tijdens specifieke multidisciplinaire overleggen (MDO’s) of infectiebesprekingen zoals reguliere overleggen tussen de arts-microbioloog en de internist-infectioloog. Bij deze patiëntcategorieën is vaak langdurig intraveneuze therapie noodzakelijk en meestal kan dit in de thuissituatie gegeven worden. Maak het antibioticabeleid tijdens deze MDO’s zo concreet mogelijk en bespreek systematisch of OPAT een optie is.
Daarnaast zijn er ook andere situaties waarbij OPAT nodig is wegens infecties door bijzonder resistente micro-organismen waarvoor geen orale opties mogelijk zijn. Hier is een belangrijke rol voor de arts-microbioloog weggelegd. Indien er een micro-organisme wordt aangetoond dat niet behandeld kan worden met orale middelen, kan de arts-microbioloog dit in de reguliere A-team besprekingen melden en kan aan de hand hiervan een OPAT-traject in gang gezet worden in overleg met patiënt en hoofdbehandelaar.
Tot slot kunnen patiënten die potentieel in aanmerking komen voor OPAT geïdentificeerd worden in ziekenhuizen met een operationeel antibioticavigilantiesysteem. Het is bijvoorbeeld praktisch om dagelijks een overzicht in het EPD te genereren van alle patiënten die reserve-antibiotica intraveneus krijgen of van patiënten die langer dan vier dagen behandeld worden met intraveneuze antimicrobiële middelen. Als er een indicatie verplicht wordt vastgelegd bij een voorschrift, kan ook dat gebruikt worden om potentieel geschikte patiënten te vinden. Denk bijvoorbeeld aan gewrichtsprothese-infecties, vaatinfecties of endocarditis. De hoofdbehandelaar kan dan benaderd worden om te kijken of de patiënt in aanmerking komt voor het stoppen of switchen van de antimicrobiële middelen en als dat niet mogelijk is voor het initiëren van een OPAT-traject.

2.2 - Initiatie van OPAT op de spoedeisende hulp, dagbehandeling of polikliniek
|
|
Het komt steeds vaker voor dat er, in ieder geval initieel, een indicatie is voor intraveneuze antibiotica, maar de patiënt niet per se opgenomen hoeft te worden. Hiervoor zijn verschillende redenen. Zo is er een toename van infecties met multiresistente bacteriën zonder goede orale behandelopties, waaronder ESBL-producerende Enterobacterales. Daarnaast vindt er een krachtige ontwikkeling plaats in de mogelijkheden van thuismonitoring, zie ook hoofdstuk 1.4.4 IT en monitoring. Deze ontwikkeling is nu nog met name te zien in de chronische setting, bij bijvoorbeeld patiënten met hartfalen of COPD, maar deze zal zich naar verwachting ook uitbreiden naar de acute setting. Denk hierbij aan patiënten die niet erg ziek zijn, maar zich wel (en vaak bij herhaling) presenteren met een gecompliceerde urineweginfectie.
Voorbeelden van groepen patiënten die niet erg ziek zijn maar zich wel presenteren op de spoedeisende hulp of polikliniek met een indicatie voor IV antibiotica zijn patiënten met bijvoorbeeld neurolues, borreliose, of een ongecompliceerde cellulitis. Tezamen zullen de uitbreiding van het indicatiegebied van OPAT zonder opname, mogelijkheden tot snelle initiatie ervan, en een kwaliteitsverbetering van de zorg thuis ervoor zorgen dat de komende jaren steeds vaker patiënten zonder een ziekenhuisopname thuis behandeld worden.
Afhankelijk van de plaats waar de patiënt zich presenteert, zal de initiatie van OPAT gebeuren via de SEH of tijdens een korte (dag-)opname, aangezien patiënten doorgaans eerst nog een intraveneuze toegang nodig hebben, de apotheek tijd nodig heeft voor de bereiding van de IV antibiotica en de specialistische wijkverpleging geregeld moet worden. Daarnaast kan door deze korte wachttijd de eerste toediening van de IV antibiotica gecontroleerd verlopen. Bij patiënten die eerder OPAT-zorg hebben ontvangen en die nog een intraveneuze toegang hebben kan een nieuw OPAT-traject in de toekomst steeds vaker direct thuis gestart worden door snelle actie van de apotheek en specialistische wijkverpleging. Daarnaast wordt het in de toekomst wellicht mogelijk om ook bij andere patiënten in de thuissituatie intraveneus antimicrobiële middelen, ook die zij nooit eerder toegediend kregen, op te starten met behulp van specialistische wijkverpleging. Hierbij zou de regie zowel bij het ziekenhuis als bij de huisarts of specialist ouderengeneeskunde, of bij een intramurale samenwerking tussen hen kunnen liggen.
2.2.1 - Initiatie op de spoedeisende hulp
Een patiënt die zich met een infectieziekte op de spoedeisende hulp (SEH) presenteert en niet opgenomen hoeft te worden maar wel intraveneuze antimicrobiële middelen dient te krijgen, komt mogelijk in aanmerking voor OPAT.
Dé uitdaging hierbij is om met de betrokken afdelingen voor de patiënt een strakke en sluitende planning te maken geconcentreerd op liefst één dagdeel. Dit vereist flexibiliteit van de radiologie (intraveneuze toegang), het transferbureau (regelen specialistische wijkverpleging), de dagopname-afdeling (de eerste toediening) en de apotheek (bereiding IV antibiotica). Om dit zo optimaal mogelijk te laten verlopen dienen er goede afspraken gemaakt te worden met deze betrokken afdelingen. Het wegnemen van belemmerende factoren en stimuleren van draagkracht binnen de afdelingen spelen hierbij ook een rol. Een OPAT-team heeft hierin een belangrijke spilfunctie en is de drijvende kracht achter het veranderproces door middel van veel uitleg en overleg.
In Nederland betreft dit nog een relatief kleine groep, maar in het buitenland is hier meer ervaring mee. Voorbeelden van indicaties zijn cellulitis door MRSA of urineweginfecties door multiresistente bacteriën. In een gerandomiseerde studie in Nieuw-Zeeland werd aan patiënten met cellulitis op de SEH een enkele dosis cefazoline gegeven, waarna intraveneuze behandeling thuis of in het ziekenhuis gecontinueerd werd. De auteurs concludeerden dat OPAT effectief en veilig was. Daarnaast zijn er succesvolle voorbeelden van OPAT-programma’s in de Verenigde Staten voor patiënten met een cellulitis die zich op de SEH presenteren. Patiënten in deze studie werden primair na een OPAT screening direct ontslagen met intraveneuze antibiotica of dit gebeurde de eerste dag van een opname op de acute opname afdeling (zie de achtergrondinformatie voor deze voorbeelden).
Uitdagingen hierbij, zeker in tijden van schaarste van personeel, kunnen zijn het organiseren van specialistische wijkverpleging en het regelen van een intraveneuze toegangsweg. Het is echter ook bij een deel van de patiënten mogelijk om op de SEH OPAT op te starten via een perifeer infuus en binnen één tot vier dagen een centraal veneuze katheter te plaatsen tijdens een korte (dag-)opname.
Toediening van de eerste dosis
Engelse en Amerikaanse richtlijnen bevelen aan dat de eerste gift van een nieuw antibioticum wordt toegediend onder toezicht van gezondheidszorgpersoneel dat bekwaam is om anafylactische reacties te herkennen en te behandelen. In de scenario’s zoals in de vorige alinea’s geschetst, vindt de toediening plaats in het ziekenhuis, waarmee per definitie gehoor wordt gegeven aan bovenstaande aanbevelingen.
In de toekomst is er een infrastructuur denkbaar waarbij OPAT buiten het ziekenhuis geïnitieerd wordt en de eerste gift in de thuissituatie gegeven wordt. De Amerikaanse IDSA richtlijn zegt dat dat mogelijk is bij een patiënt zonder bekende allergie voor een antibioticum uit dezelfde klasse en onder toezicht van een gezondheidszorgmedewerker die toegerust is om te handelen bij anafylactische reacties. De nadruk wordt hierbij gelegd op de toediening van de eerste dosis. Anafylaxie kan echter ook in een later stadium en tevens bij orale toediening optreden. In algemene zin is het risico op een anafylactische reactie echter laag (geschat 1-4 gevallen per 10.000 toedieningen).
2.3 - Beoordeling of OPAT een geschikte behandelwijze is
|
|
De noodzaak voor ziekenhuiszorg (naast IV antimicrobiële middelen) is wat met name bepaalt of iemand thuis behandeld kan worden met OPAT. De klinische toestand, de noodzaak voor specifieke interventies en de kans op complicaties spelen een belangrijke rol bij de afweging of de intraveneuze behandeling thuis voortgezet kan worden of niet. Het type infectie zelf is niet bepalend of OPAT wel of geen geschikte behandelwijze is. In principe kan iedere infectie (ten dele) in de thuissituatie behandeld worden.
2.3.1 - Beoordeling door OPAT-team
Zodra het de verwachting is dat er –naast de toediening van intraveneuze antimicrobiële middelen– binnenkort geen opname-indicatie meer is voor een bepaalde patiënt, dient beoordeeld te worden of deze patiënt in aanmerking komt voor OPAT. De Amerikaanse en Britse OPAT-richtlijnen bevelen aan dat een expert op het gebied van infectieziekten dat doet. Dit is bij uitstek dus een taak voor het OPAT-team. Beoordeling vooraf leidt mogelijk tot minder heropnames. Daarnaast blijkt, bij beoordeling door een expert, dat voor een significant deel van de patiënten toch een oraal alternatief bestaat, of dat er soms helemaal geen antibioticum geïndiceerd is.
2.3.2 - Beoordelingscriteria
Tabel 2.1 geeft een overzicht van de criteria voor de beoordeling of OPAT een geschikte behandelwijze is voor een bepaalde patiënt. Ieder OPAT-programma dient deze criteria en bijbehorende praktische aspecten inzichtelijk te maken voor de behandelaren. De minimaal vereiste fysieke en/of mentale capaciteiten van patiënten zijn niet onderzocht. Sommige studies laten associaties zien tussen patiëntkenmerken en de kans op heropname (zie tabel 3.1) en succesvolle afronding van het OPAT-traject. Deze zijn echter niet te gebruiken als hard criterium om OPAT wel of niet toe te passen, maar kunnen wel gebruikt worden voor een geïndividualiseerde afweging. Het OPAT-team zal samen met de patiënt, mantelzorgers, verpleegkundigen en hoofdbehandelaar moeten besluiten of OPAT een geschikte behandelmodaliteit is. Een ernstige visuele of manuele beperking, dementie, mentale retardatie of verslavingsproblematiek maken OPAT uitdagend, maar niet per definitie onmogelijk. Naast bovengenoemde criteria dient stilgestaan te worden bij de financiering van OPAT. Dit kan in enkele gevallen een barrière voor OPAT zijn (zie hoofdstuk 1.5 Tijdsbelasting en financiering).
2.4 - De selectie van het antimicrobiële middel
|
|
De start van een antimicrobiële behandeling in het ziekenhuis betreft meestal empirische therapie. Nadat de klinische diagnose duidelijk is geworden en de resultaten van de microbiologische diagnostiek bekend zijn, volgt een definitieve antimicrobiële behandeling. Dat is het moment waarop een definitief behandelplan opgesteld dient te worden (zie hoofdstuk 2.8 Het opstellen van een behandelplan). Dit principe geldt zowel voor de patiënt die de gehele behandelduur opgenomen blijft als voor de patiënt die OPAT ontvangt.
Bij de selectie van het antimicrobiële middel bij toediening buiten het ziekenhuis gelden in eerste instantie dezelfde criteria als tijdens opname, waarbij het gewenste geneesmiddel:
- werkzaam is tegen de verwekkers(s) van de infectie;
- een adequate concentratie bereikt op de plaats van infectie;
- een zo smal mogelijk antimicrobieel spectrum heeft;
- zo min mogelijk bijwerkingen/toxiciteit heeft;
- de laagst mogelijke kosten heeft.
2.4.1 - De noodzakelijke toedieningsfrequentie
In de Nederlandse praktijk wordt de toediening van intraveneuze antimicrobiële middelen buiten het ziekenhuis veelal uitgevoerd door gespecialiseerde wijkverpleging. Er zijn echter grenzen aan de capaciteit van de wijkverpleging. De praktijk leert dat een doseerfrequentie van meer dan tweemaal per dag veelal lastig is.
De noodzakelijke toedieningsfrequentie van een antibioticum is afhankelijk van de twee factoren:
- De farmacokinetische en farmacodynamische kenmerken van het middel
- De houdbaarheid van het antimicrobiële middel
Farmacokinetische en farmacodynamische aspecten
De noodzakelijke toedienfrequentie hangt mede af van de farmacokinetiek en de farmacodynamiek (PK/PD) van antimicrobiële middelen. Hierbij kan onderscheid gemaakt worden tussen middelen met tijdsafhankelijke en concentratieafhankelijke remming van micro-organismen. De minimale inhiberende concentratie (MIC) is hierbij een belangrijke parameter. De MIC is de laagste concentratie van het antibioticum waarbij de groei van het micro-organisme geremd wordt. In geval van tijdsafhankelijke remming is de effectiviteit afhankelijk van de tijd dat de vrije (ongebonden) concentratie van het antimicrobiële middel groter is dan de MIC (fT> MIC). Dit geldt bijvoorbeeld voor alle bètalactam-antibiotica. Dit is de reden dat middelen met een korte eliminatiehalfwaardetijd (T1/2) uit deze groep, zoals flucloxacilline en benzylpenicilline, frequent gedoseerd moeten worden in geval van intermitterende toediening. In het kader van OPAT heeft continue toediening van dergelijke middelen, indien de houdbaarheid het toelaat (zie volgende paragraaf Houdbaarheid antimicrobiële middelen), dan ook de voorkeur. Daarentegen volstaat voor bijvoorbeeld ceftriaxon, vanwege de langere T1/2, meestal een eenmaal daagse dosering.
Bij antimicrobiële middelen met concentratieafhankelijke doding of remming is de effectiviteit afhankelijk van de verhouding tussen de totale blootstelling (en eventueel piekconcentratie) aan het antimicrobiële middel en de MIC (AUC/MIC, Cmax/MIC). Tot deze groep behoren o.a. de glycopeptiden, chinolonen en aminoglycosiden. Bij deze middelen is er, in tegenstelling tot bij tijdsafhankelijke remming, geen noodzaak voor korte doseerintervallen, ook niet in het geval van een korte T1/2. Toch kan ook bij bepaalde middelen met concentratieafhankelijke doding continue toediening zinvol zijn, zoals bijvoorbeeld bij vancomycine. Vancomycine kan zowel intermitterend als continu worden toegediend. Het praktische voordeel van continue toediening is dat er slechts eenmaal per dag een handeling met de lijn noodzakelijk is. Daarnaast heeft continue toediening van vancomycine de voorkeur met het oog op therapeutic drug monitoring (TDM; zie hoofdstuk 3.1.4. Therapeutic drug monitoring), omdat bloedafname dan op ieder moment kan plaatsvinden.
Houdbaarheid antimicrobiële middelen
Bij middelen met een korte houdbaarheid door beperkte fysisch-chemische stabiliteit is continue toediening niet altijd mogelijk. In dit geval blijft intermitterende dosering noodzakelijk. Landelijk beleid m.b.t. houdbaarheden van antimicrobiële middelen is te vinden in het Handboek Parenteralia op de KNMP Kennisbank.
2.4.2 - Verschillende toedieningsvormen
Antimicrobiële middelen kunnen in de thuissituatie in verschillende toedieningsvormen gegeven worden. Hieronder volgt een beschrijving van de diverse mogelijkheden met de voor- Antimicrobiële middelen kunnen in de thuissituatie in verschillende toedieningsvormen gegeven worden. Medicatie kan toegediend worden als een infuus of als een bolusinjectie. De verschillende toedieningsvormen zijn samengevat in tabel 2.2.
Door sommige thuiszorgorganisaties kunnen eenvoudige handelingen bij het klaarmaken van medicatie zelf worden uitgevoerd. Bijvoorbeeld het optrekken van een injectievloeistof in een spuit of het oplossen van een injectiepoeder en vervolgens optrekken van de juiste dosering in de spuit en bij een infuus dit vervolgens toevoegen aan de infuuszak. Verdunningen kunnen doorgaans niet door hen gedaan worden. Het klaarmaken van een medicatiecassette of een elastomeerpomp is een complexe handeling die in de apotheek uitgevoerd moet worden. Voor het voor toediening gereed maken van medicatie moet een wijkverplegingsmedewerker wel geschoold zijn en is een dubbele controle nodig, eventueel op afstand met beeldbellen of foto’s.
Hieronder volgt een beschrijving van de diverse mogelijkheden voor het geven van een infuus met de voor- en nadelen.
Infuuszak
Dit is de toedieningsvorm die in de kliniek het meest toegepast wordt. Het grote voordeel van de infuuszak is dat deze goedkoop is ten opzichte van de andere mogelijkheden. De verpleegkundige kan dit infuus in de thuissituatie ook ter plekke klaarmaken (zie bovenstaande randvoorwaarden hierbij). Het nadeel is dat de patiënt soms gebonden is aan een infuusstandaard. De bewegingsvrijheid van de patiënt wordt hierdoor beperkt. Met name bij langlopende infusen is een infuuspaal een groot nadeel voor een patiënt die wel mobiel is. Een rugzak of tasje met een pompgestuurd infuus kan een alternatief zijn voor een infuusstandaard en dit zorgt voor meer bewegingsvrijheid van de patiënt. Toediening van het infuus kan via een mechanische pomp gedaan worden, wat een zeer nauwkeurige inloopsnelheid mogelijk maakt. De zak kan ook op basis van zwaartekracht via een druppelkamer leeglopen (vrijlopend infuus). Ook dan kan de infuussnelheid geregeld worden.
Medicatiecassette
Een medicatiecassette dient in een apotheek gevuld te worden met medicatie. Dit is een complex proces. De medicatiecassette wordt geplaatst in een pomp; het meest gebruikt is de CADD-Legay PCA-pomp, die aankomende periode vervangen zal worden door de CADD-Solis VIP-pomp. Dit is een draagbare pomp die geprogrammeerd dient te worden met de juiste gegevens. Deze pomp werkt op batterijen of een netwerkadaptor. Door de pompfunctie kan de inloopsnelheid nauwkeurig gereguleerd worden, wat van belang is bij medicatie met een nauwe therapeutische breedte. Met deze pomp kan de patiënt binnen vastgestelde grenzen extra bolussen toepassen. Deze functie is voor antimicrobiële middelen niet van belang, wel voor pijnmedicatie (PCA-functie).
Elastomeerpomp
Er zijn elastomeerpompen van meerdere leveranciers op de markt, waarbij het werkingsmechanisme voor alle pompen gelijk is. Het verschil zit hem in het uiterlijk en de behuizing van de pomp. De elastomeerpomp is een niet-elektronische medicatiepomp, speciaal ontwikkeld voor ambulante infuustherapie. De elastomeer “ballon” wordt in de apotheek gevuld met medicatie die na aansluiten langzaam met een bepaalde snelheid leegloopt en de oplossing door het slangetje de bloedvaten in duwt. Twee nadelen van elastomeerpompen is dat hun werking afhankelijk is van de positie van de pomp en de omgevingstemperatuur, en dat de infuusduur afhankelijk is van het gekozen volume in combinatie met de pomp. Juiste instructies voor gebruik zijn dus van groot belang, omdat onjuist gebruik kan leiden tot het niet goed leeglopen van de pomp met afwijkingen tot meer dan 10%. Daarnaast zijn de keuzemogelijkheden voor de infuusduur niet onbeperkt, omdat deze dus afhangt van het volume en de pomp.
Ongeacht of er aan alle voorwaarden is voldaan zal er bij toediening middels een elastomeerpomp vrijwel altijd meer spreiding zijn in infuusduur. De elastomeerpomp kan in een speciaal daarvoor geleverd heuptasje gedragen worden waardoor de bewegingsvrijheid van de patiënt niet beperkt wordt en deze optie wel heel patiëntvriendelijk is.
Bolusinjectie
Naast de diverse mogelijkheden voor toediening via het infuus kunnen bepaalde antimicrobiële middelen ook middels een bolusinjectie worden toegediend.
Voordeel van een bolusinjectie is dat de medicatie in een relatief korte tijd kan worden gegeven en dat de patiënt daarna vrij is om te bewegen en te doen wat hij kan. Bij een bolusinjectie geldt in sommige gevallen wel een minimale of maximale toediensnelheid die goed opgevolgd moet worden. Een bolusinjectie is echter niet voor alle geneesmiddelen mogelijk. Een voorbeeld van een middel waarbij een bolusinjectie uitkomst biedt is amoxicilline/clavulaanzuur. Vanwege de korte houdbaarheid kan dit niet vooraf bereid worden door de apotheek, bijvoorbeeld in een elastomeerpomp. OPAT zou dan toch mogelijk zijn als de medicatie ter plekke door de wijkverpleging wordt bereid en toegediend middels een bolusinjectie, mits de capaciteit van de wijkverpleging toereikend is voor de toedieningsfrequentie van vier keer per dag. Indien de capaciteit van de thuiszorg niet toereikend is, kan uitgezocht worden of zelftoediening van OPAT (self-administered OPAT; S-OPAT) een optie is, zie hoofdstuk 3.2 Zelftoediening.
Vanuit het OPAT-team in het Radboudumc en AUMC worden bolusinjecties sporadisch georganiseerd (enkele keren per jaar). Bolusinjecties hebben echter wel de voorkeur bij patiënten die naast antibiotica ook totale parenterale voeding (TPV) krijgen. Aangezien deze patiënten al een groot deel van de dag aan een infuus vast zitten voor hun TPV, zijn extra pompen voor het toedienen van antibiotica minder praktisch. Vaak kan dat ook niet omdat er maar één lumen beschikbaar is en dit al voor de TPV wordt gebruikt. Ook zijn deze patiënten vaak al getraind in het zelf toedienen van de TPV en zijn ze in dat geval meestal ook in staat om handelingen uit te voeren voor hun IV antibiotica.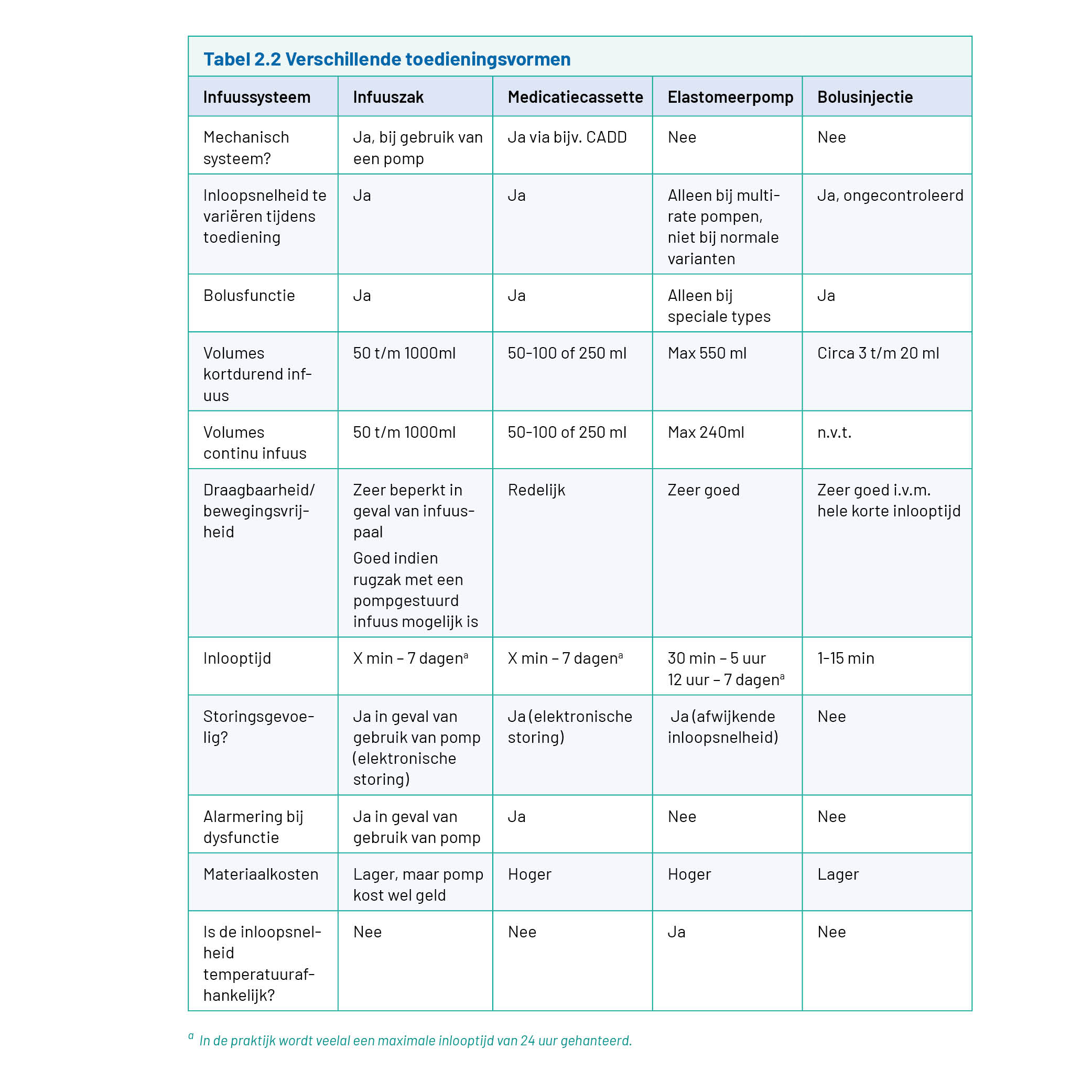

2.5 - Het informeren van patiënten en mantelzorgers
|
|
Patiëntgerichte zorg vereist, onafhankelijk van de plaats waar de patiënt zich bevindt, goede informatieverstrekking. De informatie die de verschillende zorgverleners geven dient op elkaar en al bestaande informatie te zijn afgestemd. Het verdient de aanbeveling om de bron van informatie te standaardiseren en om na mondelinge uitleg de informatie ook zoveel mogelijk schriftelijk mee te geven en/of digitaal beschikbaar te stellen. Zo ontvangt de patiënt dezelfde informatie tijdens opname en/of op de polikliniek en/of thuis.
Voorbeelden van informatievoorziening zijn de website met algemene informatie over OPAT in het Radboudumc (link: https://www.radboudumc.nl/opat) of de informatiebrieven uit het Canisius Wilhelmina Ziekenhuis, het Elisabeth-TweeSteden Ziekenhuis en het Amsterdam UMC die als bijlage 2 zijn toegevoegd.
In het gesprek met de patiënt dienen in ieder geval onderstaande zaken te worden besproken:
- Informed consent
- De intraveneuze toegangsweg
- Het antimicrobiële middel en hulpmiddel inclusief bewaarcondities en vernietiging
- Logistiek van antimicrobiële middelen en hulpmiddelen
- Follow-up en contactgegevens
Informed consent
Het opstarten van OPAT is een besluit dat samen met de patiënt genomen wordt. Naast het feit dat de omstandigheden medisch gezien geschikt moeten zijn voor OPAT, moet ook de patiënt meegenomen worden in de besluitvorming rondom het starten van OPAT. Het is van belang eventuele bezwaren of angsten in kaart te brengen en op te lossen. Hierbij is het van belang om de voor- en nadelen en de praktische invulling van OPAT te bespreken. Bij voorkeur dient ervoor gezorgd te worden dat mantelzorgers en/of familie aanwezig zijn.
De intraveneuze toegang
Geef uitleg aan de patiënt en mantelzorgers over welk type toegangsweg de patiënt heeft/gaat krijgen, welke potentiële complicaties kunnen optreden en waar zij aandacht voor moeten hebben thuis (hygiëne, verzorging). Tevens is het zaak om de patiënt te informeren over wat te doen bij problemen of vragen.
Het antimicrobiële middel en hulpmiddel inclusief bewaarcondities en vernietiging Het antimicrobiële middel en hulpmiddel inclusief bewaarcondities en vernietiging
Hierbij is van belang dat de patiënt wordt geïnformeerd over mogelijke bijwerkingen van de toe te dienen antibiotica, en hoe en wanneer deze te melden. Wettelijk gezien is de apotheek die de geneesmiddelen ter hand stelt verplicht om de patiënt te informeren over de geleverde genees- en hulpmiddelen. Juist bij OPAT-patiënten is het van belang dat de informatie wordt afgestemd op de situatie en eventueel aanwezige kennis bij de patiënt. Antimicrobiële therapie thuis bestaat vaak uit een product dat voor toediening gereed gemaakt wordt (VTGM) met één of meerdere werkzame componenten, waarbij de bijsluiter niet altijd geschikt is om (direct, zonder aanpassingen) als patiëntinformatie te verstrekken. Tevens is het belangrijk om een patiënt te informeren over de eigen verantwoordelijkheden, zoals het tijdig uit de koelkast halen van het antimicrobiële middel voorafgaand aan toediening. Twee voorbeelden van speciaal voor OPAT ontwikkelde bijsluiters uit het Maastricht UMC+ en het Radboudumc zijn toegevoegd, die standaard mee worden gestuurd aan de patiënt bij de eerste levering van de antibiotica (bijlage 3). Tot slot is het aan te bevelen om hiervoor geschikte patiënten in deze fase al te informeren over de mogelijkheid tot zelftoediening. In hoofdstuk 3.2 wordt hierop verder ingegaan.
Logistiek van antimicrobiële middelen en hulpmiddelen
Antimicrobiële middelen die al voor toediening gereed zijn gemaakt in een ziekenhuis of bereidingscentrum kunnen een korte houdbaarheid hebben, waardoor de logistiek complex kan zijn. Er zijn frequente vervolgleveringen (‘re-supply’) nodig. De frequentie van bereidingen en vervolgleveringen is niet alleen afhankelijk van de houdbaarheid van de antimicrobiële middelen (zie hoofdstuk 2.4.1. De noodzakelijke toedieningsfrequentie), maar ook van verwachte aanpassingen in de dosis en/of de toedieningsfrequentie. De bereidingsfrequentie kan bijvoorbeeld hoger liggen dan wat qua houdbaarheid mogelijk is bij middelen waarbij de dosering afhankelijk is van geneesmiddelenconcentraties zoals vancomycine (zie hoofdstuk 3.1.4. Therapeutic drug monitoring). De patiënt dient goed te worden geïnformeerd over wanneer dergelijke vervolgleveringen plaatsvinden (zie bijvoorbeeld onderaan bijlage 3). Ook dient de patiënt goed op de hoogte te zijn over wie verantwoordelijk is voor de logistiek, wat de mogelijkheden zijn en hoe contact op te nemen bij afwijkingen van logistieke afspraken. Denk bij dergelijke afwijkingen bijvoorbeeld aan wijzigingen die moeten worden doorgegeven aan de zorgverleners, zoals een ziekenhuisopname aan de bereidingsapotheek.
Follow-up en contactgegevens
Draag er zorg voor dat de patiënt en eventuele mantelzorgers vóór ontslag alle gegevens (naam, organisatie, telefoonnummer) hebben van wijkverpleging, OPAT-team, apotheek en de hoofdbehandelaar. Zorg er ook voor dat ze weten wie ze waarvoor kunnen bellen. Stem onderling af wanneer en waar het eerste zorgmoment plaatsvindt. Tevens dient, indien van toepassing, besproken te worden wanneer er een polibezoek of telefonisch consult plaats zal vinden (zie hoofdstuk 2.8 Het opstellen van een behandelplan). Informeer de patiënt ook duidelijk waar en wanneer lab te laten prikken.
2.6 - Het aanvraagproces
|
|
Na het stellen van de indicatie voor OPAT en het informeren van de patiënt over de aanvraag dienen diverse zaken geregeld te worden zoals de plaatsing van een intraveneuze toegang, voorschrift(en) voor de antimicrobiële therapieën, en de aanvraag voor de benodigde nazorg door het specialistisch team van de wijkverpleging. Bij een klinische patiënt kunnen deze zaken aangevraagd worden op het moment dat de ontslagdatum bekend is. Bij een poliklinische patiënt dient de datum van de eerste toediening, die in principe in het ziekenhuis plaatsvindt, gepland te zijn alvorens de aanvraag in te kunnen dienen. Zorg dat het aanvraagproces goed gecoördineerd wordt. Dit is bij uitstek een taak van het OPAT-team, of anders een transferverpleegkundige die nauw samenwerkt met het OPAT-team. In figuur 2.3 staat een voorbeeld van het ETZ van hoe een OPAT orderaanvraag kan worden ingericht in het EPD om het aanvraagproces te standaardiseren.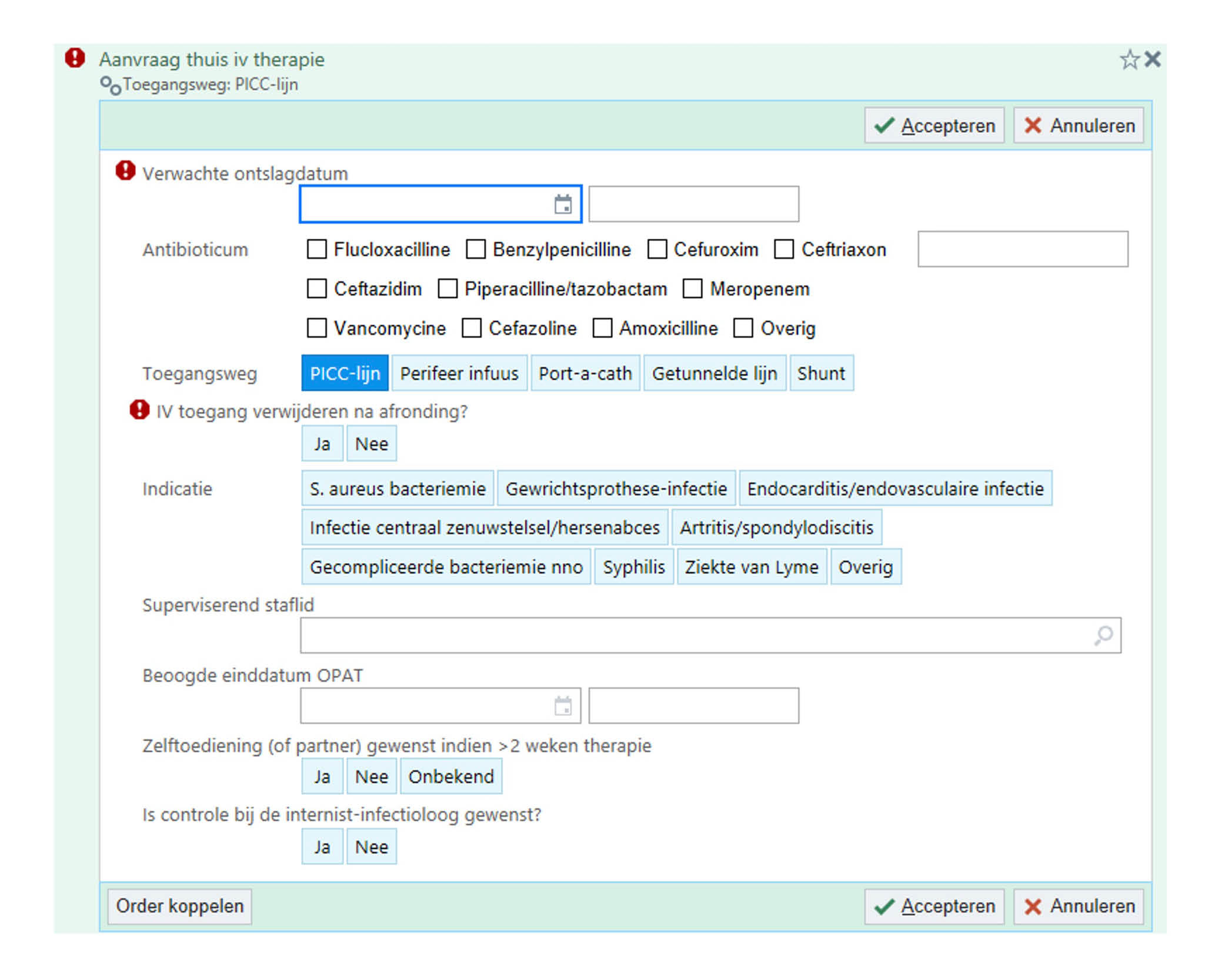
2.6.1 - Aanvraag plaatsing intraveneuze toegang
Voorafgaand aan de start van OPAT zal een intraveneuze toegang beschikbaar moeten zijn. Indien de gewenste toegang nog niet aanwezig is, zal een perifeer infuus of centraal veneuze katheter na de indicatiestelling voor OPAT geplaatst moeten worden (zie hoofdstuk 2.7 De intraveneuze toegang). De startdatum voor OPAT is daarmee mede afhankelijk van de datum waarop de intraveneuze toegang aanwezig is. Zorg dat er een heldere en efficiënte infrastructuur is voor het plaatsen van een intraveneuze toegangsweg. Dit kan belegd worden bij de interventieradioloog, maar ook andere afdelingen kunnen deze expertise hebben. Er zijn bijvoorbeeld ziekenhuizen met vooraf gereserveerde tijdsblokken bij de interventieradiologie voor eventuele OPAT-patiënten.
2.6.2 - Voorschrift voor medicatie
Net als voor elke medicamenteuze behandeling zijn er voor de intraveneuze antimicrobiële therapie in de thuissituatie voorschriften nodig. Het is belangrijk om deze voorschriften tijdig aan te leveren bij de apotheek. De apotheek heeft namelijk tijd nodig om het antimicrobiële middel voor toediening gereed te maken of in te kopen. In de praktijk kan het zinvol zijn om met gestandaardiseerde orders te werken waarbij voor veel voorkomende antimicrobiële middelen de toedienfrequentie, het volume, de inlooptijd en het oplosmiddel reeds ingevuld zijn. Figuur 2.4 toont twee voorbeelden van een gestandaardiseerd voorschrift. Geef, indien bekend, een stopdatum aan op de voorschriften. Indien de stopdatum nog niet bekend is, is het wenselijk om een herbeoordelingsmoment aan te geven. Beschrijf daarnaast de indicatie en de intraveneuze toegang en selecteer welke materialen t.b.v. de intraveneuze toediening nodig zijn. Maak tot slot, indien van toepassing, een voorschrift voor een ‘slot’ voor de gebruikte intraveneuze toegang.
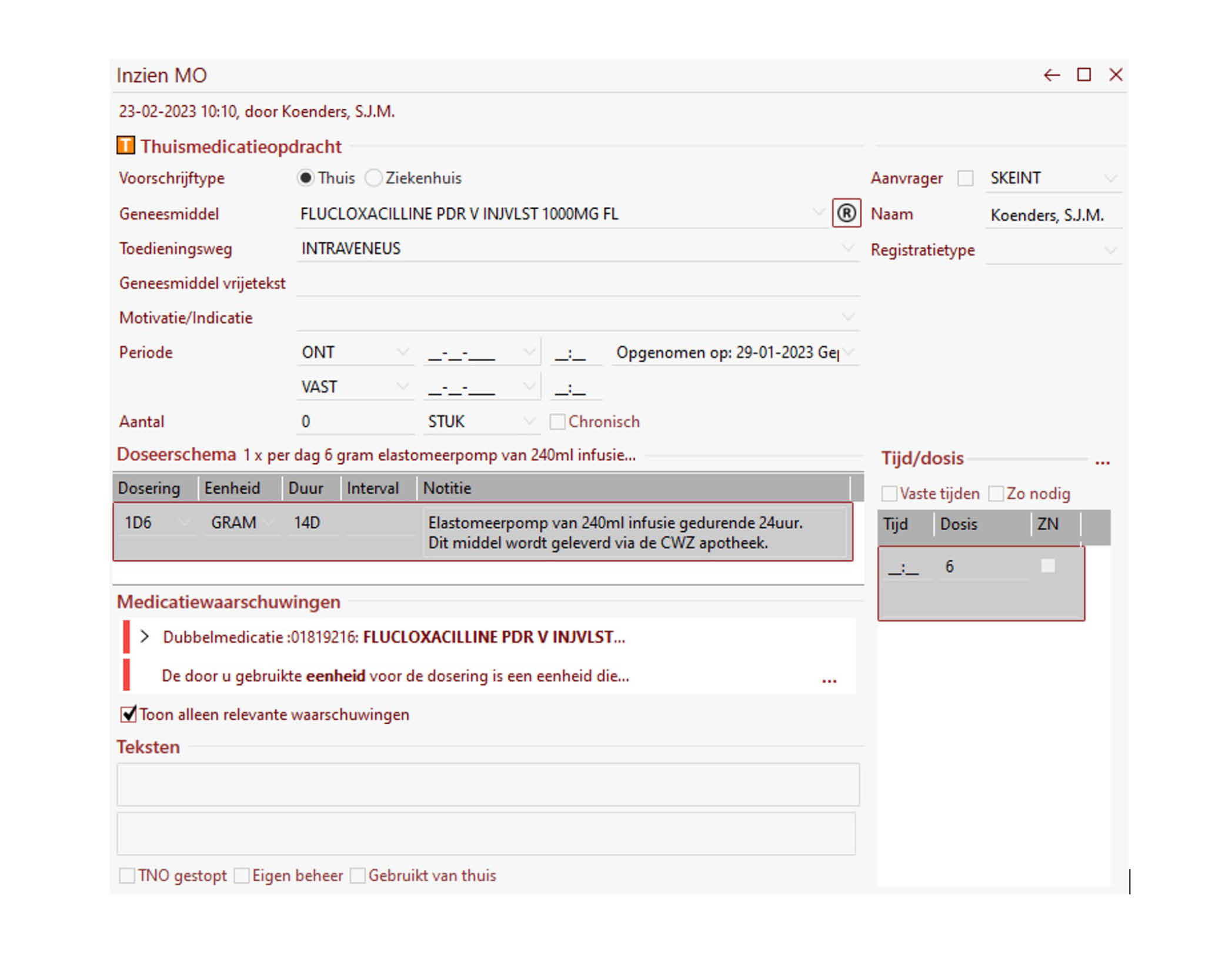
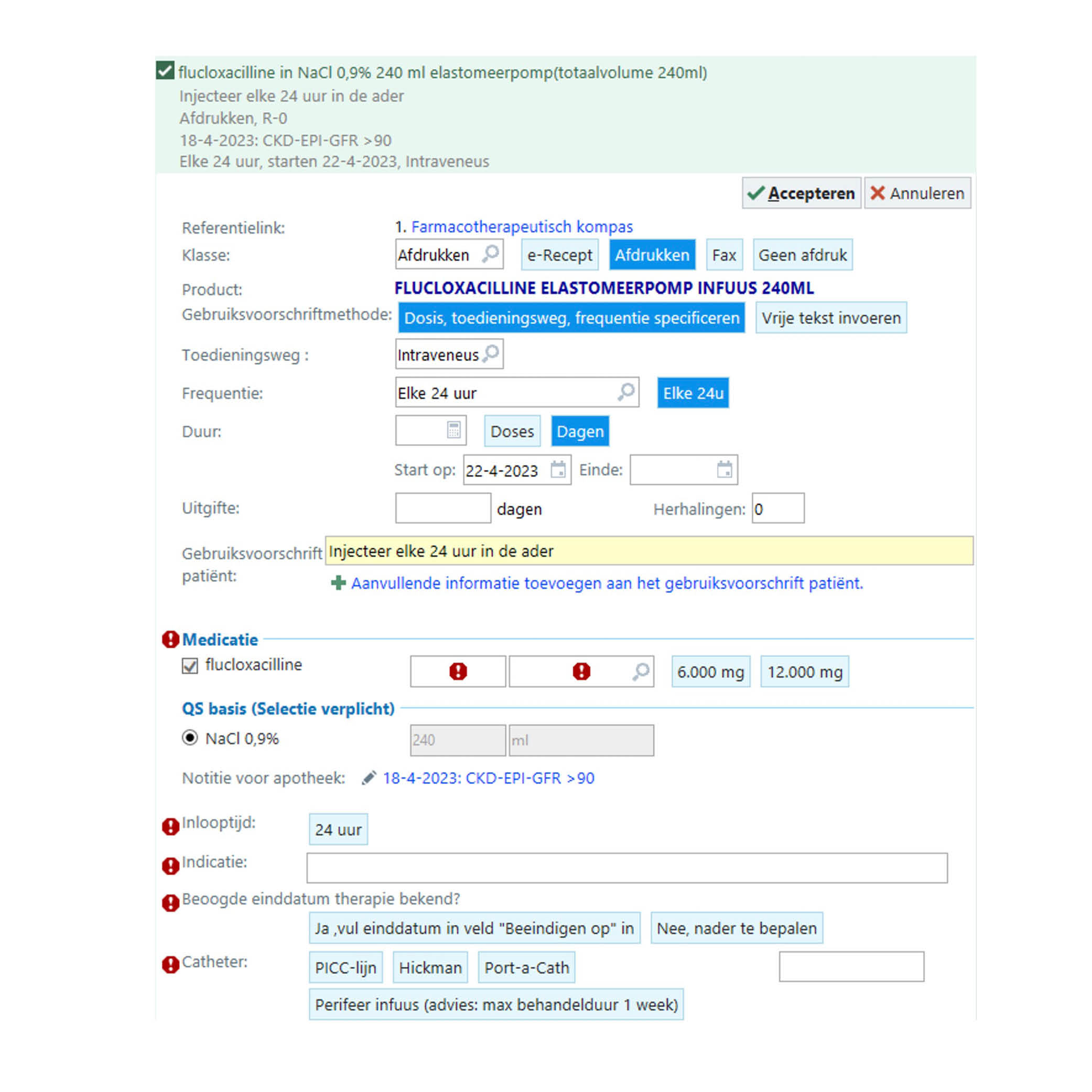
Figuur 2.4 Voorbeelden van gestandaardiseerd voorschriften uit het CWZ (HiX) en het Radboudumc (EPIC)
2.6.3 - Aanvraag voor nazorg door specialistisch team van de wijkverpleging
Veelal zullen gespecialiseerde wijkverpleegkundigen de intraveneuze toediening van antimicrobiële middelen uitvoeren en de intraveneuze toegang verzorgen in de thuissituatie. Hiervoor is het belangrijk dat tijdig een aanvraag voor nazorg wordt ingediend bij het transferpunt van het ziekenhuis. Vervolgens dient een uitvoeringsverzoek, met daarin de uit te voeren handelingen door de verpleegkundigen, te worden opgesteld. Verder dienen diverse zaken doorgegeven omschreven te worden zoals patiëntgegevens, indicatie, toedienfrequentie, startdatum en einddatum (indien bekend). Daarnaast is het belangrijk om in het uitvoeringsverzoek te noteren dat de verpleegkundige de intraveneuze toegang aan het einde van de behandeling (wel of niet) dient te verwijderen (in geval van perifeer infuus, midline of PICC), tenzij deze om andere redenen dient te blijven zitten. Het uitvoeringsverzoek en voorschrift(en) dienen vóór start van de zorg in het bezit te zijn van het specialistisch team dat de OPAT-zorg gaat leveren.
2.7 - Intraveneuze toegang
|
|
Om een patiënt thuis optimaal te kunnen behandelen, moet er goed gekeken worden naar een geschikte intraveneuze toegangsweg. Belangrijke factoren bij de keuze zijn de duur van de behandeling, de eigenschappen van het antimicrobiële middel en patiëntkarakteristieken. In de leidraad [SH1] infuustherapie is een beslisboom voor de lijnkeuze weergegeven die als ondersteuning bij de selectie van een intraveneuze toegang gebruikt kan worden. Ook zal een commissie van de V&VN aankomende jaren een richtlijn gaan ontwikkelen voor intraveneuze toediening van medicatie. Daarnaast is het belangrijk om de mogelijkheden in het eigen ziekenhuis te inventariseren en hier het lokale beleid op toe te spitsen. E is het belangrijk om dit beleid af te stemmen met thuiszorgorganisaties. Een voorbeeld van lokaal beleid omtrent de toegangswegen is hieronder te vinden in figuur 2.5 van een beslisboom veneuze toegang uit het Amsterdam UMC. 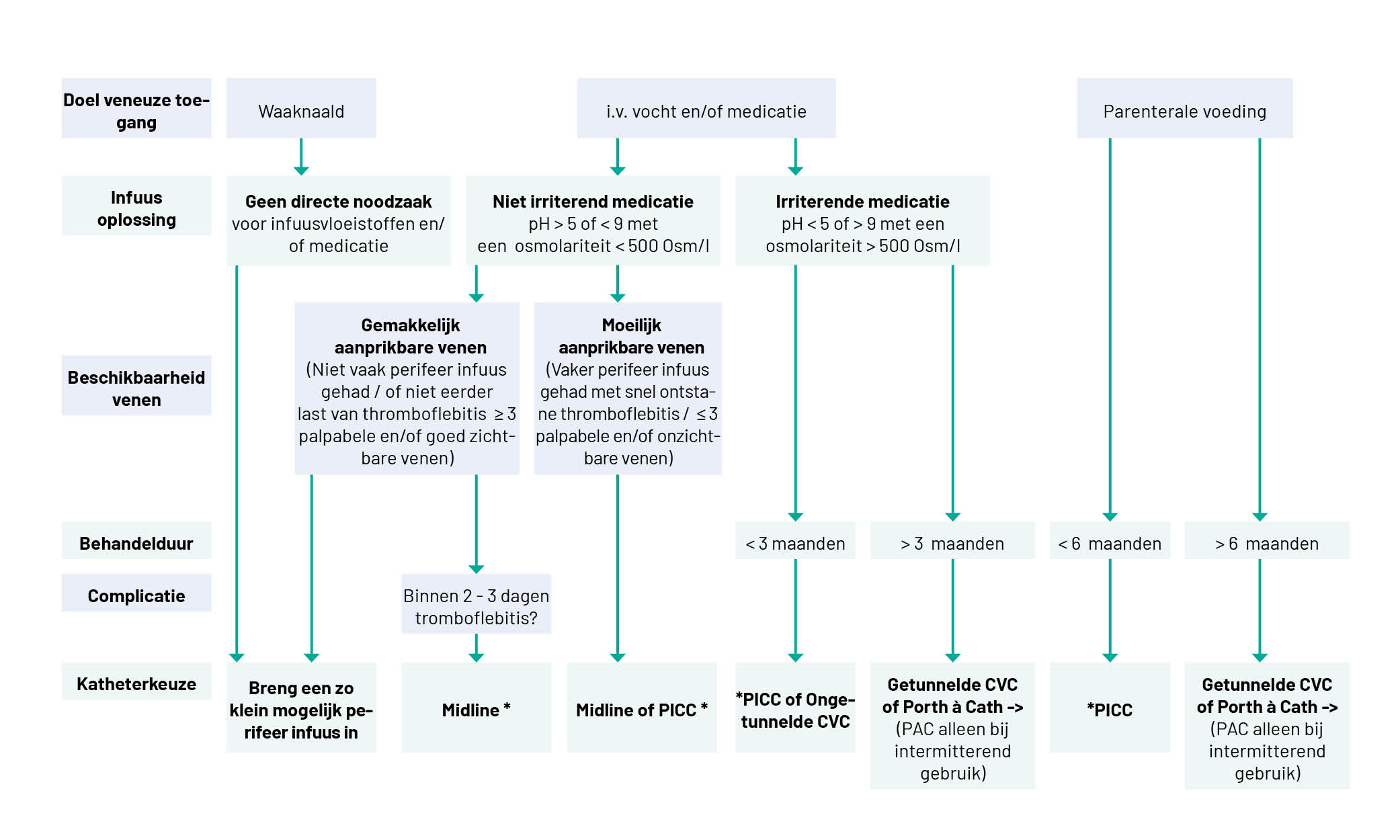
Figuur 2.5 Voorbeeld van een beslisboom (centraal) veneuze toegang Amsterdam UMC
Een overzicht van de diverse toegangswegen is weergegeven in tabel 2.3. Waar mogelijk heeft een enkellumen lijn de voorkeur, omdat dat geassocieerd is met minder complicaties. Indien een enkellumen lijn niet mogelijk is, kan het risico op minder complicaties geminimaliseerd worden door erop te letten dat het tweede lumen goed wordt geflusht, bijvoorbeeld door standaard per keer te wisselen van lumen indien er maar één lumen gebruikt hoeft te worden.
Intraveneuze toegangen worden verdeeld in centrale veneuze en niet-centraal veneuze katheters. Centraal veneuze katheters die geschikt zijn voor OPAT zijn de ‘peripherally inserted central catheters’ (in het Nederlands vaak ‘PICC’ of (foutief) ‘PICC-lijn’ genoemd), de Port-a-Cath en getunnelde centraal veneuze katheters zoals de Hickman©, Tesio© of de Broviac© katheter. Afgezien van een PICC worden ongetunnelde centraal veneuze katheters in internationale richtlijnen niet aangeraden. Perifere infusen en midlines zijn niet-centraal veneuze toegangen.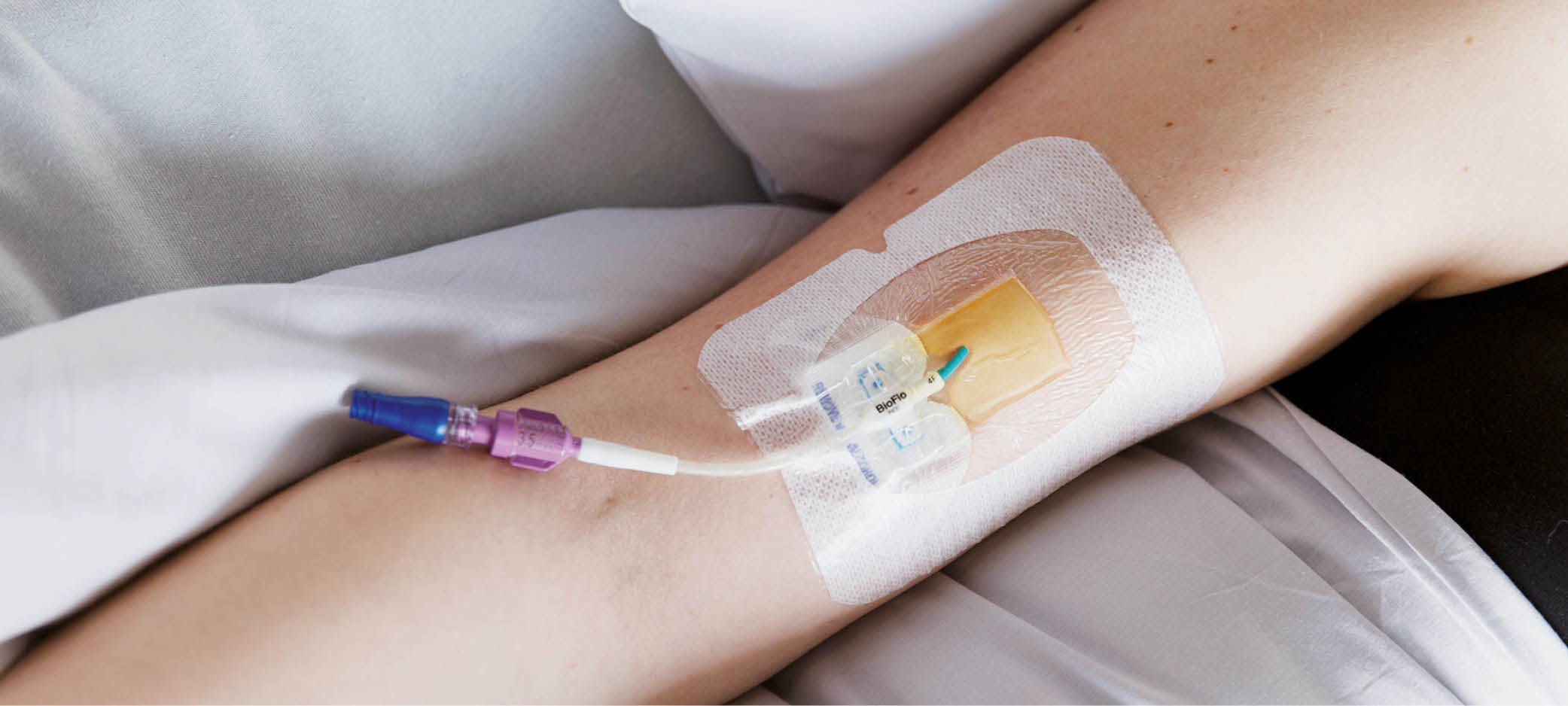
Figuur 2.6 Een voorbeeld van een PICC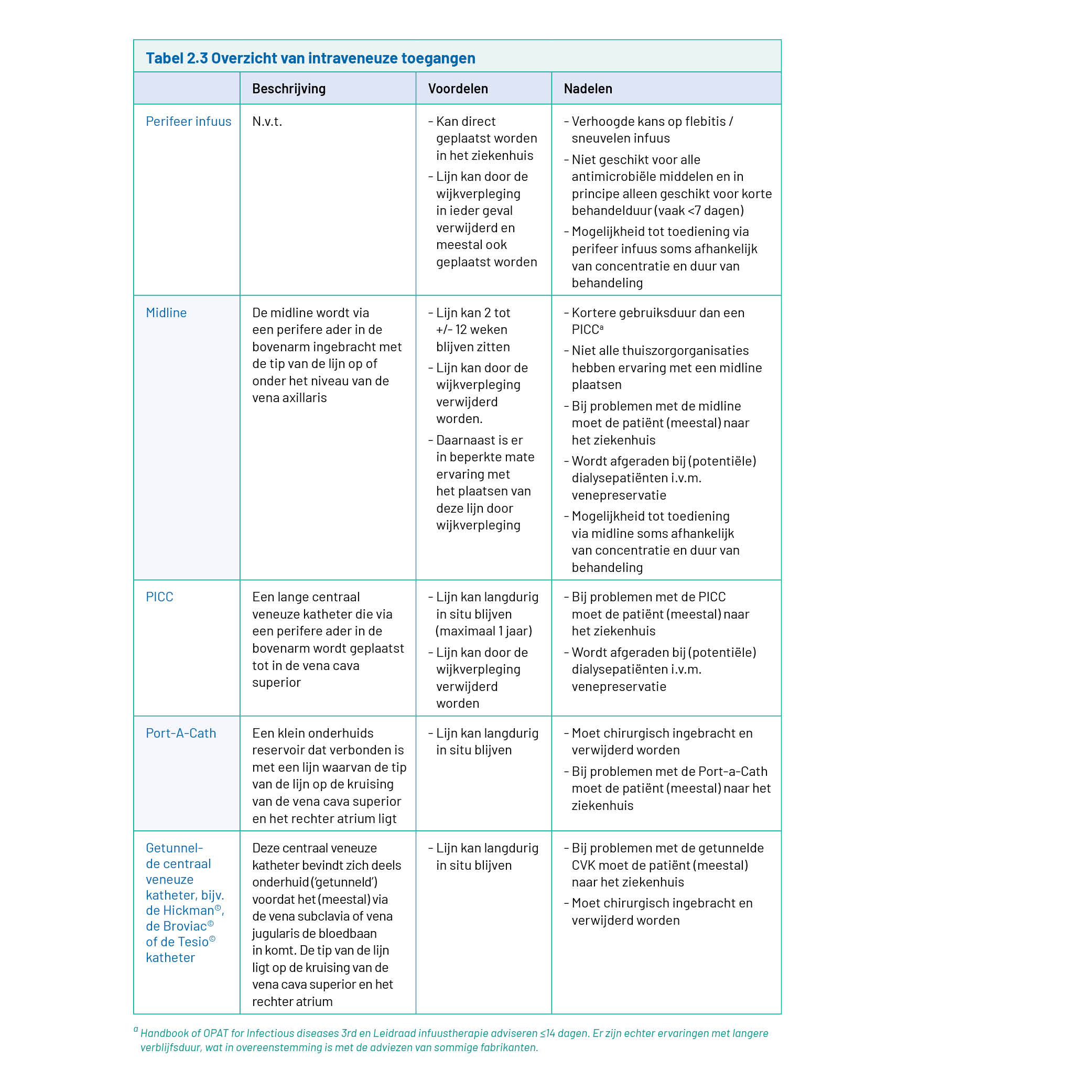
2.8 - Het opstellen van een behandelplan
|
|
De start van een antimicrobiële behandeling bij een opgenomen patiënt betreft meestal empirische therapie. Een definitieve antimicrobiële behandeling wordt ingesteld nadat de klinische diagnose en de resultaten van de microbiologische diagnostiek bekend zijn.
Het is belangrijk om een volledig behandelplan op te stellen. In tabel 2.4 staan inhoudelijke aspecten die in het behandelplan dienen te worden beschreven. Bij het opstellen van een behandelplan dient een expert (arts-microbioloog, internist-infectioloog en/of kinderarts-infectioloog) betrokken te zijn. Het behandelplan dient in samenspraak met de hoofdbehandelaar, indien dit geen infectioloog betreft, tot stand te komen en altijd te worden vastgelegd in het patiëntendossier. Spreek tevens af wie de inhoudelijke verantwoordelijkheid heeft voor het behandelplan. Daarnaast is het belangrijk om de huisarts of specialist ouderengeneeskunde over het behandelplan te informeren.  Bij start van OPAT dient vastgelegd te worden wie waarvoor verantwoordelijk is. Verschillende constructies zijn mogelijk. In Nederlandse ziekenhuizen is het vaak gebruikelijk dat de hoofdbehandelaar na initiatie van OPAT verantwoordelijk blijft en wordt eventueel bij bepaalde taken in het voortzettingstraject ondersteund door het OPAT-team. Een alternatief is dat de gehele behandeling wordt overgenomen door de infectioloog uit het OPAT-team, wat ook in enkele ziekenhuizen al de standaard is. Recente (Amerikaanse) literatuur ondersteunt het laatste model. Patiënten behandeld via door infectiologen geleide OPAT-programma’s werden minder vaak heropgenomen en hadden lagere uitgaven aan gezondheidszorgkosten.
Bij start van OPAT dient vastgelegd te worden wie waarvoor verantwoordelijk is. Verschillende constructies zijn mogelijk. In Nederlandse ziekenhuizen is het vaak gebruikelijk dat de hoofdbehandelaar na initiatie van OPAT verantwoordelijk blijft en wordt eventueel bij bepaalde taken in het voortzettingstraject ondersteund door het OPAT-team. Een alternatief is dat de gehele behandeling wordt overgenomen door de infectioloog uit het OPAT-team, wat ook in enkele ziekenhuizen al de standaard is. Recente (Amerikaanse) literatuur ondersteunt het laatste model. Patiënten behandeld via door infectiologen geleide OPAT-programma’s werden minder vaak heropgenomen en hadden lagere uitgaven aan gezondheidszorgkosten.
Literatuur
- Anderson NR. When to use a midline catheter. Nursing. 2005 Apr;35(4):28. doi: 10.1097/00152193-200504000-00049.
- Chapman ALN, Patel S, Horner C, Gilchrist M et al. Outpatient parenteral antimicrobial therapy: updated recommendations from the UK. J Antimicrob Chemother. 2019 Nov 1;74(11):3125-3127. doi: 10.1093/jac/dkz343
- Corwin P, Toop L, McGeoch G et al. Randomised controlled trial of intravenous antibiotic treatment for cellulitis at home compared with hospital. BMJ. 2005 Jan 15;330(7483):129.
- de Velde, F, Mouton JW, de Winter BCM et al. “Clinical applications of population pharmacokinetic models of antibiotics: Challenges and perspectives.” Pharmacol Res 134: 280-288. doi: 10.1016/j.phrs.2018.07.005.
- Handbook of; Outpatient Parenteral Antimicrobial Therapy For Infectious Diseases; 3ed. 2016 CRG Publishing, Division of The Curry Rockefeller Group, LLC, and the Infectious Diseases Society of America. https://www.idsociety.org/opat-ehandbook/
- Lam PW, Volling C, Chan T et al. Impact of Defaulting to Single-Lumen Peripherally Inserted Central Catheters on Patient Outcomes: An Interrupted Time Series Study. Clin Infect Dis. 2018 Aug 31;67(6):954-957. doi: 10.1093/cid/ciy301
- LEIDRAAD INFUUSTHERAPIE - De beste keuzes voor de beste zorg maken.
- Loriaux A, Desmond M, Li PC. A Primer on Home Infusion Administration Methods. Open Forum Infect Dis. 2022 Oct 7;9(12):ofac525. doi: 10.1093/ofid/ofac525.
- Mitchell ED, Czoski Murray C, Meads D et al. Clinical and cost-effectiveness, safety and acceptability of community intravenous antibiotic service models: CIVAS systematic review. BMJ Open. 2017 Apr 20;7(4):e013560. doi: 10.1136/bmjopen-2016-013560.
- Norris AH, Shrestha NK, Allison GM et al. Infectious Diseases Society of America Clinical Practice Guideline for the Management of Outpatient Parenteral Antimicrobial Therapy. Clin Infect Dis. 2019 Jan 1;68(1):e1-e35. doi: 10.1093/cid/ciy745
- Rentala M, Andrews S, Tiberio A et al. Intravenous Home Infusion Therapy Instituted From a 24-Hour Clinical Decision Unit For Patients With Cellulitis. Am J Emerg Med. 2016 Jul;34(7):1273-5. doi: 10.1016/j.ajem.2016.04.022.
- Underwood J, Marks M, Collins S et al. Intravenous catheter-related adverse events exceed drug-related adverse events in outpatient parenteral antimicrobial therapy. J Antimicrob Chemother. 2019 Mar 1;74(3):787-790. doi: 10.1093/jac/dky474.
- Wijnakker R, Visser LE, Schippers EF et al. The impact of an infectious disease expert team on outpatient parenteral antimicrobial treatment in the Netherlands. Int J Clin Pharm. 2019 Feb;41(1):49-55. doi: 10.1007/s11096-018-0751-4.
- Yadav K, Suh KN, Eagles D et al. Evaluation of an emergency department to outpatient parenteral antibiotic therapy program for cellulitis. Am J Emerg Med. 2019 Nov;37(11):2008-2014. doi: 10.1016/j.ajem.2019.02.023.
- Yagnik KJ, Steven Brown L, Saad HA et al. Implementation of IV push antibiotics for outpatients during a national fluid shortage following hurricane Maria. Open Forum Infect Dis. 2022 Mar 21;9(5):ofac117. doi: 10.1093/ofid/ofac117.
Lees verder
- Hoofdstuk 1 - Organisatie van een OPAT-programma
- Hoofdstuk 3 - Voortzetting en afronding van het OPAT-traject
- Hoofdstuk 4 - Communicatie tussen zorgverleners gedurende het OPAT-traject
- Hoofdstuk 5 - Aandachtspunten bij kinderen
- Hoofdstuk 6 - Bewaken van de kwaliteit van zorg voor OPAT-patiënten
- Hoofdstuk 7 - Bijlagen
- Download de OPAT praktijkgids
